
| A. | 常温下所有的金属都是固态 | |
| B. | 金属具有导电、导热和延展性 | |
| C. | 金属元素的原子只有还原性,离子只有氧化性 | |
| D. | 所有金属元素都以化合态存在于自然界 |
科目:高中化学 来源: 题型:选择题
| 选项 | 目的 | 试剂与方法 | 原理 |
| A | 灭火 | 混合Al2(SO4)3与NaHCO3两种溶液 | 两物质直接发生化学反应产生CO2 |
| B | 制备胆矾 | 将CuSO4溶液加热直至蒸干 | 加热促进Cu2+的水解 |
| C | 配制AlCl3溶液 | AlCl3溶液中加硫酸 | 抑制Al3+水解 |
| D | 除铁锈 | NH4Cl溶液 | NH4Cl溶液显酸性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同物质的量浓度的下列溶液中NH4+的浓度:(NH4)2SO4>NH4Cl>NH4HCO3 | |
| B. | 微粒半径:K+>S2->F- | |
| C. | 给出质子的能力:CH3COOH>C2H5OH>H2O | |
| D. | 氢化物的沸点:HF>HCl>HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
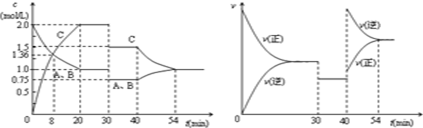
| A. | 30min时降低温度,40min时升高温度 | |
| B. | 8min时反应平衡 | |
| C. | 反应方程式中的x=1,正反应为放热反应 | |
| D. | 该反应20~30min的平衡常数比30~40min的平衡常数大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①④⑤ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Br2>Fe2+>I2 | B. | Br2>Fe3+>I2 | C. | I2>Br2>Fe3+ | D. | Fe3+>Br2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaNO3 | B. | Mg(NO3)2 | ||
| C. | AgNO3 | D. | NaNO3和AgNO3的混合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com