
已知碳化铝(Al4C3)与水反应生成氢氧化铝和甲烷。为了探究甲烷性质,某同学设计如下两组实验方案:
甲方案探究甲烷与氧化剂反应(如图1所示);
乙方案探究甲烷与氯气反应的条件(如图2所示)。
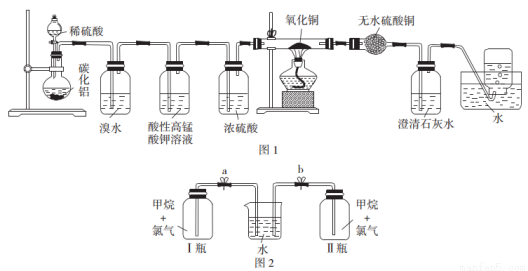
甲方案实验现象:溴水不褪色,无水硫酸铜变蓝色,澄清石灰水变浑浊。
乙方案实验操作过程:通过排饱和食盐水的方法收集两瓶甲烷与氯气(体积比为1:4)的混合气体,I瓶放在光亮处,Ⅱ瓶用预先准备好的黑色纸套套上,按图2安装好装置,并加紧弹簧夹a和b。
(1)碳化铝与稀硫酸反应的化学方程式为____________________。
(2)实验甲中浓硫酸的作用是_______________,集气瓶中收集到的气体_________(填“能”或“不能”)直接排入空气中。
(3)下列对甲方案实验中的有关现象与结论的叙述都正确的是_________(填标号)。
A.酸性高锰酸钾溶液不褪色,结论是通常条件下甲烷不能与强氧化剂反应
B.硬质玻璃管里黑色粉末无颜色变化,结论是甲烷不与氧化铜反应
C.硬质玻璃管里黑色粉末变红色,推断氧化铜与甲烷反应只生成水和二氧化碳
D.甲烷不能与溴水反应,推知甲烷不能与卤素单质反应
(4)写出甲方案实验中硬质玻璃管里可能发生反应的化学方程式:________________(假设消耗甲烷与氧化铜的物质的量之比为2:7)。
(5)一段时间后,观察到图2装置中出现的实验现象是____________________;然后打开弹簧夹a、b,观察到的实验现象是______________________。
科目:高中化学 来源:2017届河南省高三上学期9月月考化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列说法正确的是
A.1 L 0.1 mol·L-1的NH4Cl溶液中NH4+数目为0.1NA
B.标准状况下,11.2 L SO2和SO3的混合物中硫原子数为0.5NA
C.通常情况下,3.4 g NH3中共用电子对数为0.8NA
D.6.4 g Cu在足量的硫蒸气中燃烧,转移的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上学期第一次月考化学试卷(解析版) 题型:选择题
已知充分燃烧ag乙炔气体生成1mol二氧化碳气体和液态水,并放出热量bkJ,则乙炔燃烧的热化学方程式正确的是( )。
A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=-4bkJ?mol-1
B.C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l)ΔH=2bkJ?mol-1
C.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=-2bkJ?mol-1
D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=bkJ?mol-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上学期9月月考化学试卷(解析版) 题型:选择题
已知25℃时,Ksp(BaSO4)=1.1×10-10。则在5.0%的Na2SO4溶液中(假设溶液的密度为1 g·cm-3),Ba2+的最大浓度是( )
A.4.2×10-10 mol·L-1 B.8.4×10-10 mol·L-1
C.3.1×10-10 mol·L-1 D.5.8×10-10 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省咸宁市高二上学期第一次月考化学试卷(解析版) 题型:填空题
研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(1)已知:①CaCO3 (s)=CaO(s)+CO2 (g) △H= -180 kJ·mol-l;
②2CO(g)+SO2(g)=S(s)+2CO2 (g) △H= -270 kJ·mol-l
当反应②放出135 kJ热量时,处理的SO2质量为____________;若该反应放出的热量全部用于煅烧石灰石,则处理SO2时生成CO2与煅烧石灰石时生成的CO2的质量比为___________
(2)已知:CH4(g)+4NO2( g)=4NO(g)+CO2(g)+2H2O(g) △H= -560 kJ·mol-l;
CH4(g)+4NO(g)=2N2 (g)+CO2 (g)+2H2O(g) △H=-1160 kJ·mol-1;
① 若用标准状况下4.48 L CH4还原NO2生成N2,反应中转移的电子总数为_________,(用NA表示阿伏加德罗常数值),放出的热量为_________kJ。
②若1 mol CH4还原NO2时放出的热量为710 kJ,则生成的N2和NO的物质的量之比为____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省咸宁市高二上学期第一次月考化学试卷(解析版) 题型:选择题
黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2 (g) △H=xkJ·mol-l
已知:碳的燃烧热△H1=a kJ·mol-l
S(s)+2K(s)=K2S(s) △H2=b kJ·mol-1
2K(s)+N2(g)+3O2(g)=2KNO3(s) △H3 =c kJ·mol-l
则x为( )
A.c-3a-b B.3a+b-c C.a+b-c D.c-a-b
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省咸宁市高二上学期第一次月考化学试卷(解析版) 题型:选择题
原电池的电极反应式不仅与电极材料的性质有关,也与电解质溶液有关。下列说法错误的是( )
A.由Fe、Cu、FeCl3溶液组成原电池,负极反应式为Cu- 2e- =Cu2+
B.由Al、Cu、稀硫酸组成原电池,负极反应式为Al- 3e- =Al3+
C.由Al、Mg、NaOH溶液组成原电池,负极反应式为Al+4OH- -3e-=AlO2-+2H2O
D.由Al、Cu、浓硝酸组成原电池,负极反应式为Cu- 2e- =Cu2+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次段考化学卷(解析版) 题型:选择题
下列说法正确的是
A.增大反应物的浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大
B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
C.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数
D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第一次月考化学卷(解析版) 题型:选择题
下列物质中,不属于有机合成材料 的是
的是
A.聚氯乙烯 B.电木塑料 C.有机玻璃 D.钢化玻璃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com