
【题目】根据表中信息判断,下列选项正确的是 ( )
序号 | 反应物 | 产物 |
① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4… |
② | Cl2、FeBr2 | FeCl3、FeBr3 |
③ | MnO | Cl2、Mn2+… |
A. 第①组反应的其余产物只有O2
B. 第②组反应中Cl2与FeBr2的物质的量之比为1∶2
C. 第③组反应中生成1 mol Cl2,转移电子10 mol
D. 氧化性由强到弱顺序为MnO![]() >Cl2>Fe3+>Br2
>Cl2>Fe3+>Br2
【答案】B
【解析】A、反应中KMnO4→MnSO4,Mn元素化合价由+7价降低为+2价,H2O2中氧元素化合价升高,生成氧气,根据H元素守恒可知还生成水,A错误;B、由元素化合价可知,反应中只有亚铁离子被氧化,根据电子转移守恒2n(Cl2)=n(FeBr2),即n(Cl2):n(FeBr2)=1:2,B正确;C、由信息可知,MnO4-氧化Cl-为Cl2,Cl元素化合价由-1价升高为0价,转移电子的物质的量是氯气的2倍,生成1mo1Cl2,转移电子为2mo1,C错误;D、氧化剂的氧化性强于氧化产物的氧化性,由③可知氧化性MnO4->Cl2,由②可知氧化性Cl2>Fe3+,由②可知Fe3+不能氧化Br-,氧化性Br2>Fe3+,D错误。答案选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 凡是中心原子采取sp3杂化轨道成键的分子,其几何构型都是正四面体
B. H—O键键能为463 kJ/mol,即18gH2O分解成H2和O2时,消耗能量为2×463 kJ
C. sp3杂化轨道是由同一原子中能量最近的s轨道和p轨道混合起来形成的一组能量相同的新轨道
D. 凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用铬铁矿(主要成分可表示为FeO·Cr2O3,还含有Al2O3、MgCO3、SiO2等杂质)为原料制备重铬酸钾晶体和绿矾的流程如下:
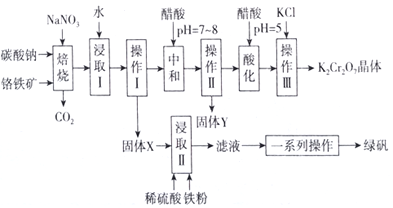
已知:Ⅰ.常见离子沉淀的pH范围
Fe3+ | Al3+ | Mg2+ | SiO32- | AlO2- | |
开始沉淀 | 1.9 | 4.2 | 8.1 | 9.5 | 10.2 |
沉淀完全 | 3.2 | 5.3 | 9.4 | 8.0 | 8.5 |
Ⅱ.焙烧过程中主要发生反应:2FeO·Cr2O3+4Na2CO3+7NaNO3=4Na2Cr2O4+Fe2O3+4CO2↑+7NaNO2。
(1)绿矾的化学式为________。
(2)焙烧后的混合物中除含有Na2Cr2O4、NaNO2和过量的Na2CO3、NaNO3外,还含有NaAlO2和Na2SiO3等物质,则焙烧过程中NaAlO2的化学方程式为___________________________。
(3)固体Y的主要成分为________(填写化学式)。
(4)酸化过程中用醋酸调节pH=5的目的为________________________;若pH调节的过低,NO2-可被氧化为NO3-,其离子方程式为_________________________________。
(5)调节pH=5后,加入KCl控制一定条件,可析出K2Cr2O7晶体,说明溶解度的大小:K2Cr2O7________Na2Cr2O7(填“大于”或“小于”)。
(6)流程中的一系列操作为____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用固体NaOH配制0.5 mol/L的NaOH溶液500 mL,有以下仪器:
①烧杯 ②100 mL量筒 ③容量瓶 ④药匙 ⑤玻璃棒 ⑥托盘天平(带砝码)⑦烧瓶
(1)配制时,必须使用的仪器有____________(填代号),还缺少的仪器是____________。
(2)在配制的转移过程中某学生进行如图操作,请指出其中的错误: _______、_______

(3)下列操作会使配制的溶液浓度偏低的是________________(填字母)
A、没有将洗涤液转移到容量瓶 B、转移过程中有少量溶液溅出
C、容量瓶洗净后未干燥 D、定容时俯视刻度线
E、固体NaOH中含有少量Na2O杂质
(4)在容量瓶使用方法中,下列操作不正确的是(填序号)____________
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用碱液润洗
C.将氢氧化钠固体直接放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
D.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】六氟化硫分子呈正八面体形(如图所示),在高电压下仍有良好的绝缘性,在电器工业方面有着广泛的用途,但逸散到空气中会引起温室效应。下列有关六氯化硫的推测正确的是

A. 六氟化硫不能燃烧
B. 六氟化硫中各原子均达到8电子稳定结构
C. 六氟化硫在水中的溶解度>六氟化硫在CS2中的溶解度
D. 六氟化硫分子是极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为短周期元素,其原子半径、化合价等信息见下表。

有关这四种元素的说法一定正确的是
A. X与W形成的化合物的电子式可表示为![]()
B. Y的氢化物能与W的氢化物反应,所得产物只含有共价键
C. X、Y能分别与氧元素形成多种氧化物
D. Z处于元素周期表中第三周期ⅣA族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com