
 ��ͼ��һ������ȼ�ϵ�ع���ʱ��ʾ��ͼ���ҳ��е������缫һ����ʯī�缫��һ�������缫������ʱ��M��N�����缫�������������٣���ش��������⣺
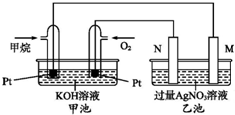
��ͼ��һ������ȼ�ϵ�ع���ʱ��ʾ��ͼ���ҳ��е������缫һ����ʯī�缫��һ�������缫������ʱ��M��N�����缫�������������٣���ش��������⣺���� ��1�����Լ׳�Ϊԭ��أ�ͨ�����ĵ缫�Ǹ�����ͨ�������ĵ缫���������ҳ�����ӵ�Դ�����ڵ��أ�����ͼƬ֪������ʱN�缫������������������������M��N�����缫�������������٣�����Ե缫��ֻ��������������NΪʯī��
��2���ҳ�Ϊ�����������Һ���缫���μӷ�Ӧ���ֱ�����Һ�������ӷŵ硢�������ŵ磻
��3��ȼ�ϵ�صĸ�������ȼ�Ϸ���ʧ���ӵ�������Ӧ��
��4�������������Һʱ��������ӦʽΪAg++e-=Ag����ϵ��ӵ�ת�Ƶ����ʵ������жϽ��м��㣮
��� �⣺��1�����Լ׳�Ϊԭ��أ�ͨ�����ĵ缫�Ǹ�����ͨ�������ĵ缫���������ҳ�����ӵ�Դ�����ڵ��أ�����ͼƬ֪������ʱN�缫������������������������M��N�����缫�������������٣�����Ե缫��ֻ��������������NΪʯī��
�ʴ�Ϊ�����أ�ʯī��������
��2���ҳ�Ϊ�����������Һ���缫���μӷ�Ӧ����Һ�������ӷŵ��������ˮ�ṩ���������ŵ������������Һ��������Ũ�����ӣ������ᣬ
�ܷ�ӦʽΪ��4AgNO3+2H2O$\frac{\underline{\;���\;}}{\;}$4Ag+4HNO3+O2����
�ʴ�Ϊ��4AgNO3+2H2O$\frac{\underline{\;���\;}}{\;}$4Ag+4HNO3+O2����
��3��������ȼ�ϵ�صĸ���������ʧ���ӵ�������Ӧ�����Ի����£��缫��ӦʽΪ��CH4-8e-+10OH-=CO32-+7H2O��
�ʴ�Ϊ��CH4-8e-+10OH-=CO32-+7H2O��
��4��n��Ag��=$\frac{2.16g}{108g/mol}$=0.02mol������Ag++e-=Ag��֪ת�Ƶ���Ϊ0.02mol���׳���ͨ������һ��Ϊ��������ӦʽΪ��CH4-8e-+10OH-=CO32-+7H2O��������n��CH4��=$\frac{0.02mol}{8}$��V��CH4��=$\frac{0.02}{8}$mol��22.4L/mol=0.056L=56mL�������ҳط�Ӧ��ϵ��4Ag��4e-��4HNO3��ת��0.02mol���ӣ�����������Ϊ0.02mol������ʱ�ҳ���Һ�����Ϊ400mL�����ҳ���H+�����ʵ���Ũ��Ϊ$\frac{0.02mol}{0.4L}$=0.05mol/L��
�ʴ�Ϊ��56��0.05mol/L��
���� ���⿼����ԭ���ԭ���͵���ԭ������ȷԭ��غ͵��ص缫�Ϸ�����Ӧ�����ͼ��ɷ�������⣬�ѶȲ���ע��缫��Ӧʽ����д��������Һ��������йأ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���õ��ķ������ԴӺ�ˮ�л�ȡ��ˮ | |
| B�� | ��ˮ�к�����Ԫ�أ�ֻ�辭������������仯�Ϳ��Եõ��嵥�� | |
| C�� | ��ˮ�����ƺ��εĹ���ֻ�����˻�ѧ�仯 | |
| D�� | �Ӻ�ˮ����þʱ�����ú�̲�ϵı�����Ca��OH��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 7.5 mL 2mol/L MgCl2��Һ | B�� | 30 mL 1mol/L KCl��Һ | ||
| C�� | 10 mL 3mol/L NaCl��Һ | D�� | 30 mL 0.5 mol/L AlCl3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

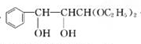 ��
�� +2Ag��NH3��2OH$\stackrel{��}{��}$
+2Ag��NH3��2OH$\stackrel{��}{��}$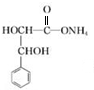 +2Ag��+3NH3+H2O��
+2Ag��+3NH3+H2O��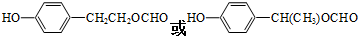 �� ����дһ�֣�
�� ����дһ�֣�
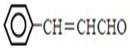 ����ƺϳ���·�������Լ���ѡ�����ϳ���·ʾ��ͼʾ�����£�CH3CH2OH$��_{170��}^{Ũ����}$CH2=$\stackrel{Br_{2}}{��}$CH2BrH2Br��
����ƺϳ���·�������Լ���ѡ�����ϳ���·ʾ��ͼʾ�����£�CH3CH2OH$��_{170��}^{Ũ����}$CH2=$\stackrel{Br_{2}}{��}$CH2BrH2Br���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | a�ֱ���b��c��d�γɵĶ�Ԫ��������a�Ļ��ϼ۾�Ϊ+1 | |
| B�� | b����������Ԫ�ؾ����γ��������ֶ�Ԫ������ | |
| C�� | a��b�γɵĻ�������һ��ֻ�й��ۼ���b��c�γɵĻ�������һ��ֻ�����Ӽ� | |
| D�� | ԭ�Ӱ뾶��С˳��d��c��b��a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ǡ����ۺ���ά�طֱ�Ϊͬ���칹�� | |
| B�� | ��ij�л����������г��ȼ������CO2��H2O���ʵ�����ȣ�����л�������ϩ | |
| C�� | ȼ�����顢�����飨C3H6��������壬��������CO2����һ��С��ȼ����ͬ�����ı�ϩ��������CO2 | |
| D�� | ��ͬ��������ϩ���Ҵ��������г��ȼ�գ����ĵ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4�� | B�� | 5�� | C�� | 6�� | D�� | 7�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ��PH���� | B�� | ��Һ�е�Zn2+Ũ������ | ||
| C�� | ��Һ�е�SO42- Ũ������ | D�� | ��Һ���ܶ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֪S��g��+O2��g���TSO2��g����H1��S��s��+O2��g���TSO2��g����H2�����H1����H2 | |
| B�� | HCl��NaOH��Ӧ���к��ȡ�H=-57.3kJ•mol-1����H2SO4��Ba��OH��2��Ӧ���к��ȡ�H=2����-57.3��kJ•mol-1 | |
| C�� | ��֪C��ʯī��s��=C�����ʯ��s����H��0������ʯ��ʯī�ȶ� | |
| D�� | ������ȼ����Ϊ285.5 kJ•mol-1����ˮ�ֽ���Ȼ�ѧ����ʽΪ��2H2O��l���T2H2��g��+O2��g����H=+285.5 kJ•mol-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com