
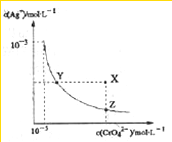
 ��t��ʱ��Ag2CrO4���ٺ�ɫ����ˮ�еij����ܽ�ƽ��ƽ��������ͼ��ʾ����֪t��ʱAgCl��Ksp=4��10-10������˵������ȷ���ǣ�������
��t��ʱ��Ag2CrO4���ٺ�ɫ����ˮ�еij����ܽ�ƽ��ƽ��������ͼ��ʾ����֪t��ʱAgCl��Ksp=4��10-10������˵������ȷ���ǣ�������| c(CrO42-) |
| c2(Cl-) |
| Ksp(Ag2CrO4) |
| Ksp2(AgCl) |
| 10-9 |
| (4��10-10)2 |
|
| 4��10-10 |
| 10-3 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��t��ʱ��ijBa��OH��2��ϡ��Һ��c��H+��=10-a mol/L��c��OH-��=10-b mol/L����֪a+b=12�������Һ����μ���pH=c�����ᣨt�棩����û����Һ�IJ���pH���±���ʾ��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
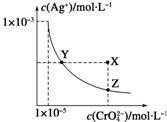 ��t��ʱ��Ag2CrO4���ٺ�ɫ����ˮ��Һ�еij����ܽ�ƽ��������ͼ��ʾ����֪AgCl��Ksp=1.8��10-10������˵������ȷ���ǣ�������
��t��ʱ��Ag2CrO4���ٺ�ɫ����ˮ��Һ�еij����ܽ�ƽ��������ͼ��ʾ����֪AgCl��Ksp=1.8��10-10������˵������ȷ���ǣ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡij�ص���ѧ2012�����10���¿���ѧ���� ���ͣ�021
|
��t��ʱ��Ag2CrO4(�ٺ�ɫ)��ˮ�еij����ܽ�ƽ��ƽ��������ͼ��ʾ����֪t��ʱAgCl��Ksp��4��10��10������˵������ȷ����
| |
A�� |
��t��ʱ��Ag2CrO4(s)��2Cl��(aq) |
B�� |
��t��ʱ����0.001 mol/L��AgNO3��Һ�ζ�20 mL��0.001 mol/L��KCl��0.001 mol/L��K2CrO4�Ļ����Һ��Cl���ȳ��� |
C�� |
��t��ʱ��Ag2CrO4��KspΪ1��10��8 |
D�� |
�ڱ�����Һ�м���K2CrO4��ʹ��Һ��Y�㵽X�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ģ���� ���ͣ�������ѡ����
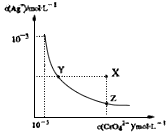
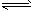 2AgCl(s)+CrO42-��aq��ƽ�ⳣ��K=6��25��107
2AgCl(s)+CrO42-��aq��ƽ�ⳣ��K=6��25��107�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com