
同温同压下,两种气体的体积如果不相同,请你推测其主要原因是( )
A.气体的分子大小不同 B.气体的物质的量不同
C.气体分子的化学性质不同 D.气体分子间的平均距离不同
科目:高中化学 来源: 题型:选择题
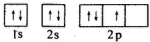
| A. | 洪特规则 | B. | 泡利原理 | C. | 能量最低原理 | D. | 洪特规则特例 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上月考一化学卷(解析版)) 题型:选择题
若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是
A.生成了一种强酸弱碱盐
B.弱酸溶液和强碱溶液反应
C.强酸溶液和弱碱溶液反应
D.一元强酸溶液和一元强碱溶液反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:实验题

(1)写出下列仪器的名称:a:__________
(2)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是_____________,将仪器补充完整后进行实验,冷凝水由___________(填f或g)口通入。
(3)现需配制0.lmol/LNaOH溶液450mL,装置II是某同学转移溶液的示意图。
①图中的错误是________________。除了图中给出的仪器和托盘天平外,为完成实验还需要的仪器有:_____________。
②根据计算得知,需称量NaOH的质量为_________g。
③配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)______ ______。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
④下列操作使配制的NaOH溶液浓度偏低的有_________。
A.称量氢氧化钠时间过长 B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线 D.定容时俯视刻度线
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:选择题
在标准状况下,mg气体A与ng气体B的分子数相同,下列说法中不正确的是( )
A.两种气体A与B的相对分子质量之比为m:n
B.同质量气体A与B的分子数之比为n:m
C.同温同压下,A、B两气体的密度之比为n:m
D.相同状况下,同体积A、B两气体的质量之比为m:n
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  +Cl2$\stackrel{光照}{→}$ +Cl2$\stackrel{光照}{→}$ +HCl +HCl | |
| B. | 2CH3CH2OH+O2 $→_{△}^{催化剂}$ 2CH3CHO+2H2O | |
| C. | ClCH2CH=CH2+NaOH $→_{△}^{H_{2}O}$ HOCH2CH=CH2+NaCl | |
| D. |  +HONO2$→_{△}^{浓硫酸}$ +HONO2$→_{△}^{浓硫酸}$ +H2O +H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
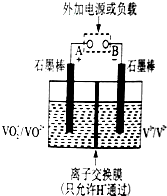 钒(V)及其化合物在工业催化、新材料和新能源等领域中有广泛的应用.回答下列问题:
钒(V)及其化合物在工业催化、新材料和新能源等领域中有广泛的应用.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1+Q2>Q3 | B. | Q1+Q2<Q3 | C. | Q1+Q2>2Q3 | D. | Q1+Q2<2Q3 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:选择题
下列各物质中所含有的分子数最多的是( )
A.标准状况下11.2 L氯气 B.17g氨气(NH3)
C.1.204×l024个H2O分子 D.0.8mol氧气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com