
 .
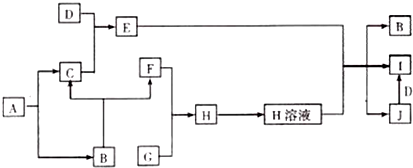
.分析 A、B常温下均为无色液体,且均由两种相同的元素组成,A生成B和C,C为气体,一般为H2O2生成H2O的反应,则A为H2O2,B为H2O,C为O2,G为黄绿色气体,应为Cl2,D是应用最广泛的金属,应为Fe,由转化关系可知F为H2,H为HCl,E为Fe3O4,J为FeCl3,I为FeCl2,结合对应单质、化合物的性质以及题目要求解答该题.
解答 解:A、B常温下均为无色液体,且均由两种相同的元素组成,A生成B和C,C为气体,一般为H2O2生成H2O的反应,则A为H2O2,B为H2O,C为O2,G为黄绿色气体,应为Cl2,D是应用最广泛的金属,应为Fe,由转化关系可知F为H2,H为HCl,E为Fe3O4,J为FeCl3,I为FeCl2,
(1)由以上分析可知A为H2O2,故答案为:H2O2;
(2)H为HCl,为共价化合物,电子式为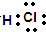 ,故答案为:
,故答案为: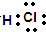 ;
;
(3)B为H2O,可在电解的条件下生成氧气和氢气,方程式为2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑,故答案为:2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑;
(4)J为FeCl3,I为FeCl2,FeCl3与Fe反应生成FeCl2,离子方程式为2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+.
点评 本题考查无机物的推断,为高频考点,侧重考查元素化合物知识的综合理解和运用,把握过氧化氢、铁等物质的性质及其转化、电解原理等为解答的关键,注意A、B、J为解答的突破口,综合性较强,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测液体积(mL) | HCl溶液体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 10.00 | 0.50 | 20.51 |
| 第二次 | 10.00 | 4.00 | 24.00 |
| 第三次 | 10.00 | 5.11 | 25.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0 mol•L-1 KNO3溶液:H+、Fe2+、SCN-、SO42- | |
| B. | 水电离出的c(H+)=10-10 mol•L-1的溶液:K+、Ba2+、NO3-、Cl- | |
| C. | pH=0的溶液:Al3+、Ag(NH3)2+、Cl-、SO42- | |
| D. | c(ClO-)=1.0 mol•L-1的溶液:Na+、SO32-、S2-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气是黄绿色气体,有毒,有刺激性气味,氯水还可杀菌消毒 | |
| B. | 液氯就是氯气的水溶液,它能使干燥的有色布条褪色 | |
| C. | 红热的铁丝在Cl2中燃烧产生棕色的雾;H2在Cl2中燃烧火焰呈淡蓝色 | |
| D. | 氯水长时间放置会变质,是因为氯气几乎完全挥发,剩下的就是水. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 合成氨工业对工、农业生产和国防都有重要意义.
合成氨工业对工、农业生产和国防都有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ⅠA | Ⅷ | ||||||
| ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| ② | ③ | ④ | ⑧ | ||||
| ⑤ | ⑥ | ⑦ | ⑨ | ||||
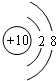
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1×10-7 mol/L | B. | 1×10-12mol/L | C. | 1×10-2 mol/L | D. | 1×10-7 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
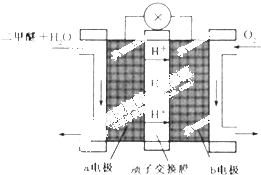 二甲醚(CH3OCH3)被称为21世界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
二甲醚(CH3OCH3)被称为21世界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com