
科目:高中化学 来源: 题型:
下面的排序不正确的是( )
A.电负性的大小: Cl>S>Al>Mg
B.硬度由大到小: 金刚石>碳化硅>晶体硅
C.熔点由高到低:石英>食盐>干冰>钠
D.晶格能由大到小:NaF> NaCl> NaBr>NaI
查看答案和解析>>
科目:高中化学 来源: 题型:
已知复分解反应:2 CH3COOH+Na2CO3==2CH3COONa+ H2O+CO2↑可自发进行。在常温下,测得浓度均为0.1mol/L的下列六种溶液的pH:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH值 | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
请你判断下列反应不能成立的是:
A.CO2 +H2O+ NaClO== NaHCO3+HClO
B.CO2 +H2O+ 2NaClO== Na2CO3+2HClO
C.CH3COOH+ NaCN== CH3COONa+HCN
D.CH3COOH+ NaClO== CH3COONa+ HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
2003年诺贝尔化学奖授予了美国科学家Peter Agre和Roderick Mackinnon以表彰他们在“水通道”和“离子通道”的研究成就。Mackinnon教授的研究内容主要是Na+、K+体积很接近,但在生物体内呈现的差别却高达1万倍,他革命性的让科学家观测Na+、K+在进入离子通道前、通道中以及穿过通道后的状态,可为病人在“离子通道”中寻找具体的病因,并研制相应药物。下列关于钠、钾的说法正确的是
A.单质钠的密度比钾的密度小 B.Na+和K+常用作氧化剂
C.钠和钾都是短周期元素 D.钠和钾的合金[ω(K)=50%~80%]在室温下呈液态
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是实验室制备氯气并进行一系列性质探究的实验装置(夹持及加热仪器已省略)。
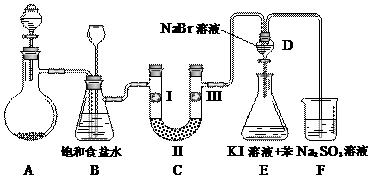
(1)用二氧化锰和浓盐酸制备氯气,则反应的离子方程式为: 。
(2)实验装置B的作用之一是除去氯气中的杂质氯化氢作用之二是起安全瓶的作用,当长颈漏斗中液面上升时,说明 ,此时应停止实验。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中II可放入 (填编号)。
A.碱石灰 B.硅胶 C.浓硫酸 D.无水氯化钙
(4)写出装置F中相应的离子反应方程式: 。
(5)设计装置D、E的目的是比较氯、溴、碘的非金属性,有人认为该设计不能达到实验目的,其理由是 。某兴趣小组的同学思考后将上述D、E、F装置改为如下图装置替代。已知当溴水浓度较小时,溶液颜色与氯水相似也呈黄色。
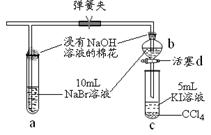
实验操作步骤如下:
I、打开弹簧夹,缓缓通入氯气
II、当a和b中的溶液都变为黄色时,夹紧弹簧夹。
III、当a中溶液由黄色变为棕色时,停止通氯气。
Ⅳ、______________________________________。
①设计步骤III的实验思想是 。
②步骤Ⅳ的操作是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列性质的比较中,正确的是
A.熔点:Li>Na>K>Rb B.沸点:NH3<PH3<AsH3<SbH3
C.热稳定性:CH4>PH3>H2O>HF D.酸性:HClO>H2SO4>H3PO4>H2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
将下列晶体熔化:氢氧化钠、二氧化硅、氧化钙、四氯化碳,需要克服的微粒间的相互作用①共价键 ②离子键 ③分子间作用力,正确的顺序是
A.①②②③ B.②①②③ C.②③②① D.①①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷
和氧气,其总反应为:2C2H6+702+8KOH 4K2C03+10H20,有关此电池的推断正确的
4K2C03+10H20,有关此电池的推断正确的
是( )。
A.负极反应为:14H20+702+28e- 280H-
280H-
B.放电一段时间后,负极周围pH升高
C.每消耗1 mol C2H6,则电路上转移的电子为14 mol
D.放电过程中KOH的物质的量浓度不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com