
����Ŀ�����������[��NH4��2Fe��SO4��26H2O]�Ƿ�����ѧ����Ҫ���Լ���ѧϰС��̽����ֽ���
��1�����鰴��ͼ1��ʾ��װ�ý���ʵ�飬�ر�ֹˮ�в�����A�е���������粒������ֽ���ȫ��������ֽ��� 
��װ��B���������� �� �����Լ��� ��
��װ��C�пɹ۲쵽�������� �� �ɴ˿�֪��������淋ķֽ�������� �� ��д��ѧʽ��
��2������ѡ�ü���ʵ���е�װ��A��ͼ2��ʾ��װ�ý���ʵ����֤��������立ֽ�IJ����л���SO2��SO3 �� ������ͬѧ��ʵ��װ���У��������ӵĺ���˳����װ�õ���ĸ��ʾ��ΪA����ȡ������������粒�����A�У�ͨ��һ��ʱ��N2�ر�ֹˮ���ٵ�ȼ�ƾ��ƣ�ͨ��N2��Ŀ���� ��
��װ��H���а�ɫ��������֤���ֽ����������G�з�����Ӧ�����ӷ���ʽΪ ��
��3�����齫һ�����������������500��ʱ������������һ��ʱ������������������ʵ��֤�����˹�����ﲻ���������� ��
���𰸡�
��1������ܣ���ʯ�ң���Һ����ɫ���ɫ��NH3
��2��DHEGF���ž�װ���еĿ�������O2������ֹ��SO2����֤�������ţ�SO3��SO2+2H2O2+Ba2+=BaSO4��+H2O+2H+
��3��ȡ�����������Թ��У���ϡ�����ܽ⣬�ٵ���KMnO4��Һ��KMnO4��Һ����ɫ
���������⣺��1����װ��B����״�����ÿ�֪Ϊ����ܣ�ʢ�Ź������������������[��NH4��2Fe��SO4��26H2O]�ֽ���ܵIJ���Ϊ����������������ˮ�����鰱������װ��C�еķ�̪��Һ������װ��B�dz�ȥ���ɵ����������Ϊ��ʯ�ң� ���Դ��ǣ�����ܣ���ʯ�ң���װ��C�пɹ۲쵽�������DZ��ɫ����������ˮ����һˮ�ϰ��������Һ�е����Լ��ԣ�������̪���ɫ��֤���ֽ�����������˰�����
���Դ��ǣ���Һ����ɫ���ɫ��NH3����2��������ѡ�ü���ʵ���е�װ��A��ͼ2��ʾ��װ�ý���ʵ����֤��������立ֽ�IJ����л���SO2��SO3 �� �ֽ����ͨ��װ��D��ֹ������ͨ��װ��H�е�����Ԫ�غ��Ȼ�����Һ�����Ƿ����������к���������ͨ��װ��E�������������Ƿ������ͨ��װ��G��������������������Ϊ���ᣬ��ϱ��������ɰ�ɫ���������ʣ���������������Ҫβ�����գ�������������֪װ������˳��ΪADHEGF��ȡ������������粒�����A�У�ͨ��һ��ʱ��N2�ر�ֹˮ���ٵ�ȼ�ƾ��ƣ�Ŀ���Ǹɾ�װ���е���������Զ����������ĸ��ţ�
���Դ��ǣ�DHEGF���ž�װ���еĿ�������O2������ֹ��SO2����֤�������ţ�
��װ��H���а�ɫ������˵�������˲�����ˮ����������ij���Ϊ���ᱵ������ԭ������������SO3 �� G�й��������������������������ᣬ������Ȼ�����Ӧ�������ᱵ��ɫ��������Ӧ�����ӷ���ʽΪ��SO2+2H2O2+Ba2+=BaSO4��+H2O+2H+ ��
���Դ��ǣ�SO3 ��SO2+2H2O2+Ba2+=BaSO4��+H2O+2H+����3�����ö��������Ӿ��л�ԭ�����ʵ����飬ʵ�����Ϊ��ȡ�����������Թ��У���ϡ�����ܽ⣬�ٵ���KMnO4��Һ��KMnO4��Һ����ɫ�����Դ��ǣ�ȡ�����������Թ��У���ϡ�����ܽ⣬�ٵ���KMnO4��Һ��KMnO4��Һ����ɫ��


 ����˼ά�żӿ���ϵ�д�
����˼ά�żӿ���ϵ�д� �����Ծ�ϵ�д�
�����Ծ�ϵ�д� �ο�����������100��ϵ�д�
�ο�����������100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��������¼��ȷ����
A. ���³�ѹ�²��1 mol N2������Ϊ28 g
B. ����Ͳ�����ˮ���ռ��Ƶõ��������Ϊ50.28 mL
C. ����ֻ250 mL������ƿ����0.1 mol��L��1500 mL��NaOH��Һ
D. ��������ƽ��ȡ2.50 g���������ȳ��ʧˮ������������0.90 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����pH=1����ɫ��Һ�У����������ܴ���������ǣ� ��
A.NH4+��Ba2+��NO3����CO32��
B.Fe2+��OH����SO42����MnO4��
C.K+��Mg2+��NO3����SO42��
D.Na+��Fe3+��Cl����AlO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���Ӧ2A(g)![]() B(g)(����ӦΪ���ȷ�Ӧ)���ܱ������дﵽƽ�⣬ƽ���c(A)/c(B)��a�����ı�ijһ�������㹻ʱ���Ӧ�ٴδﵽƽ��״̬����ʱc(A)/c(B)��b������������ȷ����( )
B(g)(����ӦΪ���ȷ�Ӧ)���ܱ������дﵽƽ�⣬ƽ���c(A)/c(B)��a�����ı�ijһ�������㹻ʱ���Ӧ�ٴδﵽƽ��״̬����ʱc(A)/c(B)��b������������ȷ����( )
A���ڸ��¶��£������ݻ��̶����䣬�������ڲ�����B���壬��a<b
B����a��b����ı���������ʹ���˴���
C���������������䣬�����¶ȣ�����a<b
D���������¶ȡ�ѹǿ���䣬����������壬����a>b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�0.1mol/L CH3COONa��ҺpH=9��������˵����ȷ���ǣ� ��
A.��������NaOH�������ҺpHС��9
B.��ˮϡ�ͣ�CH3COONaˮ��̶�����c��OH��������
C.����Һˮ�������c��OH�����T10��9
D.CH3COOH�ڳ�����Ka��ֵԼΪ1��10��5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ܱ������з������з�Ӧ��N2(g)��3H2(g)![]() 2NH3(g)(����ӦΪ���ȷ�Ӧ)����ͼ��ijһʱ��η�Ӧ�����뷴Ӧ���̵Ĺ�ϵ����ͼ��
2NH3(g)(����ӦΪ���ȷ�Ӧ)����ͼ��ijһʱ��η�Ӧ�����뷴Ӧ���̵Ĺ�ϵ����ͼ��

(1)t1��t3��t4ʱ�̣���ϵ�зֱ���ʲô���������˱仯��
t1________��t3________��t4________��
(2)����ʱ����У����İٷֺ�����ߵ���( )
A��0��t1 B��t2��t3
C��t3��t4 D��t4��t5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�����Ϊ2 L���ܱ������У������·�����Ӧ��Fe(s)+CO2(g)![]() FeO(s)+CO(g)������CO2��CO�����ʵ���(mol)��ʱ��(min)�ı仯��ϵ��ͼ��ʾ��
FeO(s)+CO(g)������CO2��CO�����ʵ���(mol)��ʱ��(min)�ı仯��ϵ��ͼ��ʾ��
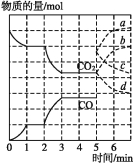
(1)��Ӧ��1 minʱ��һ�δﵽƽ��״̬�����������������3.2 g����CO2��Ũ�ȱ仯��ʾ�ķ�Ӧ����v(CO2)= ��
(2)��Ӧ������2 minʱ����ֻ�ı��¶ȣ����߷����ı仯��ͼ��ʾ��3 minʱ�ٴδﵽƽ�⣬��H 0(�>����<����=��)��
(3)5 minʱ�ٳ���һ������CO(g)��ƽ�ⷢ���ƶ�������˵����ȷ���� (��д���)��
A.v(��)��������С B.v(��)�ȼ�С������
C.v(��)��������С D.v(��)�ȼ�С������
��ʾn(CO2)�仯�������� (��дͼ�����ߵ���ĸ���)��
(4)���ù�̬���ʵ��й���������˵���÷�Ӧ�Ѿ��ﵽ��ѧƽ��״̬�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�����˵����ȷ���ǣ� ��
A.pHֵ��Ϊ4��ϡ�����NH4Cl��Һ�У�ˮ�ĵ���̶���ͬ
B.Ũ�Ⱦ�Ϊ0.1mol/L�Ĵ����NaOH��Һ�������Ϻ�lg[ ![]() ]=0
]=0
C.�ں�Ũ�ȶ�Ϊ0.01mol/L��Cl����CrO42���Ļ����Һ�еμ�AgNO3��Һ���ȳ��ֳ�������AgCl��[��֪��Ksp��AgCl��=1.8��10��10 �� Ksp��Ag2CrO4��=1.9��10��12]
D.Ũ�Ⱦ�Ϊ0.1mol/L��NH4Cl��CH3COONH4��Һ�У�c��NH4+����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���ݻ��ɱ���ܱ������з�����Ӧ��3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)��
Fe3O4(s)+4H2(g)��
�ش�����������
��1������Fe����������Ӧ���� (���������С�����䡱����ͬ)��
��2�����������ݻ���Сһ��������Ӧ���� ���淴Ӧ���� ��
��3�������������ݻ�����������N2ʹ��ϵѹǿ����������Ӧ���� ���淴Ӧ���� ��
��4������ѹǿ����������N2ʹ�������ݻ�����������Ӧ���� ���淴Ӧ���� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com