
| 3.84g |
| 64g/mol |
| 2.24L |
| 22.4L/mol |


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:高中化学 来源: 题型:阅读理解
| V-11.2n |
| 33.6n |
| V-11.2n |
| 33.6n |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
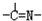 三种基团,无环状结构,三种基团的数目关系为n3=
三种基团,无环状结构,三种基团的数目关系为n3=

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
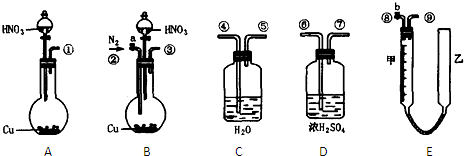
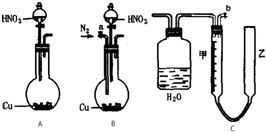
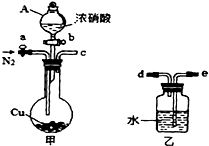 (2012?宁德模拟)某化学课外小组利用如图实验装置(夹持仪器略去),探究铜与浓硝酸反应是否有NO生成.
(2012?宁德模拟)某化学课外小组利用如图实验装置(夹持仪器略去),探究铜与浓硝酸反应是否有NO生成.查看答案和解析>>
科目:高中化学 来源:2011-2012学年福建省宁德市高三毕业班质量检查化学试卷 题型:实验题
(13分)
某化学课外小组利用下图实验装置(夹持仪器略去),探究铜与浓硝酸反应是否有NO生成。

请回答下列问题:
(1)仪器A的名称是 。
(2)甲装置的c应该与乙装置的 连接(填“d”或“e”)。
(3)乙装置中反应的化学方程式是 。
(4)实验步骤如下:
i仪器组装完毕,检查装置的气密性,加入试剂。打开旋塞a,通入N2一段时间后,关闭旋塞a。
ii打开旋塞b,滴入xmol·L-1浓硝酸V mL,充分反应后冷却,固体仍有剩余。
iii用NaOH溶液滴定乙装置中溶液,得溶质的物质的量为n mol。
①步骤i通入N2的目的是________
②为了准确测定甲装置中产生NO2的量,在步骤ii和iii之间应补充的操作是:
。
③当xV×l0-3 3n(填“>”、“=”或“<”),则证明铜与浓硝酸反应时有NO生成。
④该实验设计中存在一个明显的缺陷是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com