
| A. |  | B. |  | ||
| C. |  | D. |  |
分析 核磁共振氢谱中峰值数等于有机物中氢原子的种类数,核磁共振氢谱中只给出一种峰,说明该分子中的H原子都是等效的,只有1种H原子,等效氢判断:①同一碳原子上的氢原子是等效的,②同一碳原子上所连接甲基上的氢原子是等效的,③处于同一对称位置的碳原子上的氢原子是等效的.
解答 解:核磁共振氢谱中只给出一种峰,说明该分子中的H原子都是等效的,只有1种H原子.
A. 中3个甲基H原子都连接C原子,所处化学环境相同,只有1种H原子,核磁共振氢谱中有1个峰,故A正确;
中3个甲基H原子都连接C原子,所处化学环境相同,只有1种H原子,核磁共振氢谱中有1个峰,故A正确;
B. 中3个碳原子H原子和羟基氢原子连接不同的原子,所处化学环境不相同,有4种H原子,核磁共振氢谱中有4个峰,故B错误;
中3个碳原子H原子和羟基氢原子连接不同的原子,所处化学环境不相同,有4种H原子,核磁共振氢谱中有4个峰,故B错误;
C. 中左边碳上的H原子和中间H原子连接不同的原子,所处化学环境不相同,有2种H原子,核磁共振氢谱中有2个峰,故C错误;
中左边碳上的H原子和中间H原子连接不同的原子,所处化学环境不相同,有2种H原子,核磁共振氢谱中有2个峰,故C错误;
D. 中甲基H原子和中间H原子连接不同的原子,所处化学环境不相同,有2种H原子,核磁共振氢谱中有2个峰,故D错误.
中甲基H原子和中间H原子连接不同的原子,所处化学环境不相同,有2种H原子,核磁共振氢谱中有2个峰,故D错误.
故选A.
点评 本题考查核磁共振氢谱,难度不大,清楚核磁共振氢谱中峰值数等于有机物中氢原子的种类数.


科目:高中化学 来源: 题型:选择题
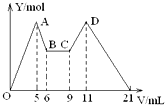 向MgCl2、AlCl3的混合溶液开始滴加6mol/L的试剂A,之后改滴试剂B,所得沉淀物质的量Y(mol)与试剂体积V(mL)间的关系如图所示.以下结论不正确的是( )
向MgCl2、AlCl3的混合溶液开始滴加6mol/L的试剂A,之后改滴试剂B,所得沉淀物质的量Y(mol)与试剂体积V(mL)间的关系如图所示.以下结论不正确的是( )| A. | 从6到9,相应离子反应方程式为H++OH-=H2O | |
| B. | A 是NaOH,B是盐酸,且c(NaOH):c( HCl)=2:1 | |
| C. | 原混合液中,c(Al3+):c(Mg2+):c(Cl-)=1:1:5 | |
| D. | A是盐酸,B是NaOH,且c(NaOH)=2c (HCl) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
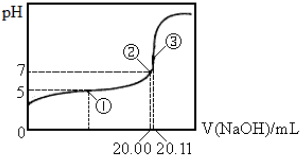
| A. | 该温度下CH3COOH的电离平衡常数约为1.8×10-5 | |
| B. | 点①处溶液中c(CH3COO-)<c(CH3COOH) | |
| C. | 点③处溶液中c(OH-)=c(CH3COOH)+c(H+) | |
| D. | 滴定过程中不可能出现:c(CH3COOH)>c(CH3COO-)>c(OH-)>c(Na+)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)拆开1mol H-H键、1mol N-H键、1mol N=N键分别需要吸收的能量为436KJ,391KJ,946KJ,求:则①1molN2生成NH3需要放出(吸收或放出)热量92KJ;
(1)拆开1mol H-H键、1mol N-H键、1mol N=N键分别需要吸收的能量为436KJ,391KJ,946KJ,求:则①1molN2生成NH3需要放出(吸收或放出)热量92KJ;查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 达到平衡时X浓度为0.04 mol•L-1 | |
| B. | 将容器体积变为20 L,Z的平衡浓度变为0.015 mol•L-1 | |
| C. | 若升高温度,X的体积分数增大,则该反应的?△H<0 | |
| D. | 若增大压强,平衡向正反应方向移动,平衡常数变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 简单离子半径:W>Y>Z | |
| B. | X与Y可形成既含极性键又含非极性键的化合物 | |
| C. | Z与W形成的化合物一定是离子化合物 | |
| D. | Y的氧化物对应的水化物的酸性一定比W的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核裂变或聚变中化学能转变为核能 | B. | 该核裂变中质子数守恒 | ||
| C. | Ba是人工核反应制得的超铀元素 | D. | ${\;}_{42}^{106}$Mo中含有106个中子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com