
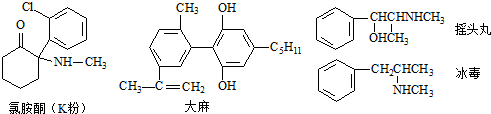
| A. | 四种毒品中都含有苯环,都属于芳香烃 | |
| B. | 摇头丸经消去、加成反应可制得冰毒 | |
| C. | 1mol大麻与溴水反应最多消耗4mol Br2 | |
| D. | 氯胺酮分子中环上所有碳原子可能共平面 |
分析 A.均含至少3种元素,而烃只含C、H元素;
B.摇头丸制得冰毒,先发生-OH的消去反应,再与氢气加成;
C.大麻中酚-OH的2个邻位与双键与溴水反应;
D.氯胺酮分子中,苯环上C原子共面,但环己酮结构中含5个四面体构型的C原子.
解答 解:A.均含至少3种元素,而烃只含C、H元素,则均不属于芳香烃,故A错误;
B.摇头丸制得冰毒,先发生-OH的消去反应,再与氢气加成,反应类型分别为消去反应、加成反应,故B正确;
C.大麻中酚-OH的2个邻位与双键与溴水反应,则1mol大麻与溴水反应最多消耗3mol Br2,故C错误;
D.氯胺酮分子中,苯环上C原子共面,但环己酮结构中含5个四面体构型的C原子,则环己酮结构中C原子不可能共面,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重酚、烯烃、醇的性质及迁移应用能力的考查,选项D为解答的难点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 烷烃的沸点随碳原子数增加而逐渐升高 | |
| B. | 任何烷烃分子中碳氢原子个数比都是相同的 | |
| C. | 丙烷与Cl2发生取代反应后生成的一氯代物不只是一种 | |
| D. | 正丁烷的熔点、沸点比异丁烷的高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2(g)和3molH2(g) | 1molCH3OH和1molH2O(g) |
| 平衡时c(CH3OH) | c1 | c2 |
| 平衡时能量变化 | 放出29.4kJ | 吸收akJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H6和C4H10一定是同系物 | |
| B. | C2H4和C4H8一定是同系物 | |
| C. | 相对分子质量相等的两种物质,不一定是同分异构体 | |
| D. | 在常温常压下,C4H10是气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
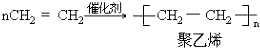 ;反应类型加聚反应.
;反应类型加聚反应.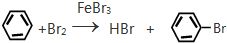 ;反应类型取代反应.
;反应类型取代反应.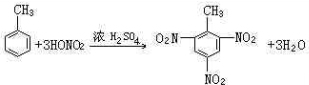 ;反应类型硝化反应(取代反应).
;反应类型硝化反应(取代反应).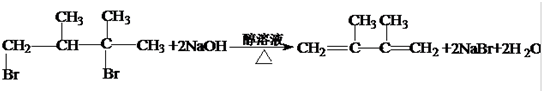 ;反应类型消去反应.
;反应类型消去反应.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 酸性 HClO4>HBrO4>HIO4 | B. | 碱性 Ba(OH)2>Ca(OH)2>Mg(OH)2 | ||
| C. | 非金属性 F>Cl>Br | D. | 稳定性 HCl>H2S>PH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 序号 | 金属 质量/g | 金属 状态 | c(H2SO4)/mol•L-1 | v(H2SO4)/mL | 溶液温度/℃ | 金属消失的时间/S | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
| 4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
| 6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 7 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
| 8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | 丝 | 1.1 | 50 | 20 | 44 | 40 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com