
科目:高中化学 来源:2015-2016学年湖南省邵阳市高一上学期第三次月考化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A.Cu溶于稀HNO3:Cu+2H++NO3-===Cu2++NO2↑+H2O
B.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-===Fe(OH)2↓
C.用CH3COOH溶解CaCO3:CaCO3+2H+===Ca2++H2O+CO2↑
D.向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2-+2H2O===Al(OH)3↓+HCO3-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二上学情调查化学试卷(解析版) 题型:填空题
(1)25℃时,浓度为0.1 mol•L-1的6种溶液①HCl ②CH3COOH ③Ba(OH)2 ④Na2CO3 ⑤KCl ⑥NH4Cl溶液pH由小到大的顺序为_________________(填写编号)。
(2)已知25℃时,CH3COOH电离常数Ka=1.7×10-5mol/L,则:
①该温度下CH3COONa的水解平衡常数Kh=__________ mol•L-1(保留到小数点后一位);
②将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的pH=7,则NH3•H2O的电离常数Ka=____,混合后溶液中离子的浓度由大到小的顺序为__________________。
(3)25℃时,将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后,溶液的pH=7,则溶液中
c(CH3COO-)+c(CH3COOH)=_________;m与n的大小关系是m___________n(填“>”“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上12月月考化学试卷(解析版) 题型:选择题
已知HCN(aq)与NaOH(aq)反应生成1 mol正盐的ΔH=-12.1 kJ/mol;强酸、强碱的稀溶液反应的中和热ΔH=-57.3 kJ/mol。则HCN在水溶液中电离的ΔH等于
A.-69.4 kJ/mol B.-45.2 kJ/mol
C.+69.4 kJ/mol D.+45.2 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上学期第五次模拟理综化学试卷(解析版) 题型:选择题
碱性硼化钒(VB2)—空气电池工作时反应为:4VB2 + 11O2=4B2O3 + 2V2O5。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( )
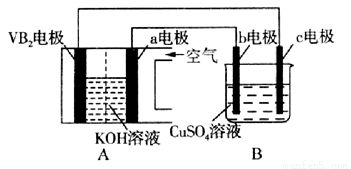
A.电解过程中,c电极表面先有红色物质析出,然后有气泡产生
B.VB2电极发生的电极反应为:2VB2 + 11H2O - 22e-=V2O5 + 2B2O3 + 22H+
C.外电路中电子由c电极流向VB2电极
D.若B装置内的液体体积为200 mL,则CuSO4溶液的物质的量浓度为0.1 mol/L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
金属镍有广泛的用途。粗镍中含有少量杂质Fe、Zn、Cu、Pt,可用电解法制备高纯度的镍(已知:氧化性Fe2+<Ni2+<Cu2+),下列叙述正确的是( )。
A.阳极发生还原反应,其电极反应式:Ni2++2e-=Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市高二上学期第三次月考化学试卷(解析版) 题型:选择题
最简式相同,但既不是同系物,又不是同分异构体的是( )
①辛烯和3-甲基-1-丁烯 ②苯和乙炔 ③1-氯丙烷和2-氯丙烷 ④甲基环己烷和乙烯
A.①② B.②③ C.③④ D.②④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西钦州港经济开发区中学高二上12月月考化学试卷(解析版) 题型:简答题
简答下列问题:
(1)酸雨是怎样形成的?它有什么危害?
(2)建筑物中的哪些金属受酸雨破坏的程度较小?
(3)为什么冬天雨水的酸性通常较强?
查看答案和解析>>
科目:高中化学 来源:2016届福建省闽粤联合体高三上学期第三次联考化学试卷(解析版) 题型:填空题
硼氢化钠(NaBH4)在化工等领域具有重要的应用价值,某研究小组采用偏硼酸钠NaBO2为主要原料制备NaBH4,其流程如下:
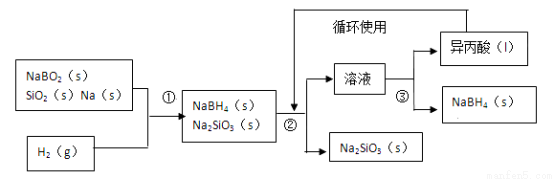
已知:NaBH4常温下能与水反应,可溶于异丙酸(沸点:13℃)。
(1)在第①步反应加料之前,需要将反应器加热至100℃以上并通入氩气,该操作的目的是: 。
(2)请配平第①步反应的化学方程式:
NaBO2+ SiO2+ Na+ H2———— NaBH4+ Na2SiO3
(3)第②步操作需要的玻璃仪器有: ;第③步分离出NaBH4并回收溶剂,采用的操作方法是 。
(4)NaBH4与水反应生成NaBO2,且反应前后B的化合价不变,该反应的化学方程式为: ,反应消耗1molNaBH4时转移的电子数目为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com