
| A.分子晶体中分子间作用力越大,分子越稳定 |
| B.原子晶体中共价键越强,熔点越高 |
| C.金属晶体发生形变时,金属键发生断裂 |
| D.氯化钠熔化时离子键未被破坏 |
科目:高中化学 来源:不详 题型:填空题
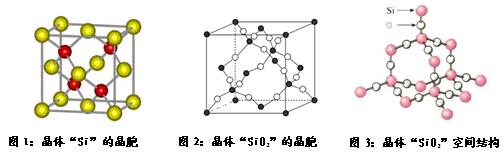
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
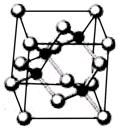
| A.砷化镓晶胞结构与NaCl相同 | B.第一电离能 As>Ga |
| C.电负性 As>Ga | D.原子半径 As>Ga |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金刚石、食盐、玻璃和水晶都是晶体 |
| B.晶体的分子(或原子、离子)排列是有规则的 |
| C.单晶体和多晶体有固定的熔点,非晶体没有固定的熔点 |
| D.单晶体和多晶体的物理性质是各向异性的,非晶体是各向同性的 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子化合物一定为离子晶体 |
| B.同周期主族元素的原子半径或离子半径都是从左至右减小 |
| C.氢氧化铁胶体带正电荷,加入电解质会产生红褐色沉淀 |
| D.两个非金属元素的原子之间形成的化学键只能是共价健 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
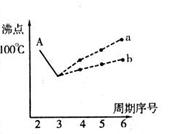
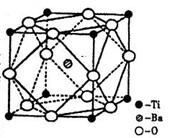

| A.氙的含量比较丰富 | B.氙的相对原子质量大 |
| C.氙原子半径大,电离能小 | D.氙原子半径小,电负性大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 氧化物 | MgO | CaO | SrO | BaO |
| 晶格能/ kJ·mol-1 | 3791 | 3410 | 3223 | 3054 |
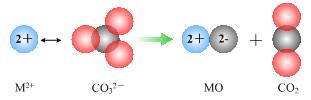
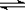 NH4++OH-,当氨水冷却时,可以将NH3·H2O和2NH3·H2O等晶体沉淀出来。
NH4++OH-,当氨水冷却时,可以将NH3·H2O和2NH3·H2O等晶体沉淀出来。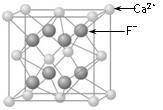
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com