
1833年,瑞典化学家阿伦尼乌斯提出酸碱电离理论,他认为:电离时产生的阳离子全部是氢离子的化合物是酸;电离时产生的阴离子全部是氢氧根离子的化合物是碱。根据此理论可知下列化合物属于酸的是( )
①NaHCO3 ②CH3COOH ③HCOOH ④NH3
⑤CH3COOC2H5 ⑥NH4Cl
A.①② B.②③
C.④⑤ D.②⑥
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列化合物的核磁共振氢谱中出现三组峰的是()
A. 2,2,3,3﹣四甲基丁烷 B. 2,3,4﹣三甲基戊烷
C. 3,4﹣二甲基己烷 D. 2,5﹣二甲基己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质或离子检验的叙述正确的是 ( )
A.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+
B.气体通过无水硫酸铜,粉末变蓝,证明原气体中含有水蒸气
C.灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,无K+
D.将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,向纯水中加入NaOH,使溶液的pH为11,则由NaOH电离出的OH﹣离子浓度与水电离的OH﹣离子浓度之比为()
A. 1010:1 B. 5×109:1 C. 108:1 D. 1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上冶炼金属一般用热分解法、热还原法和电解法。选用不同方法冶炼不同金属的主要依据是( )
A.金属在自然界中的存在形式
B.金属元素在地壳中的含量
C.金属阳离子得电子的能力
D.金属熔点的高低
查看答案和解析>>
科目:高中化学 来源: 题型:
海水占地球总储水量的97.2%,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源。
(1)海水中存在大量的氯化钠,氯化钠中的金属元素位于元素周期表________族。
(2)目前,国际上使用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经冷却而得高纯度淡水。由此可判断蒸馏法是________(填“物理变化”或“化学变化”)。
(3)工业上利用电解饱和食盐水可制得重要化工产品。反应式为NaCl+H2O—→NaOH+H2↑+Cl2↑(未配平),该反应的化学方程式是__________________________________;利用电解所得气体制36.5%的浓盐酸1 000 t,最少需消耗食盐________t。
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学做元素周期律性质递变规律实验时设计了一套实验方案,并记录了有关实验现象,见下表。请从下表实验现象(Ⅱ)中选出与方案(Ⅰ)对应的实验现象,将其序号(A、B…)填入(Ⅲ)中,并写出相应的化学方程式。
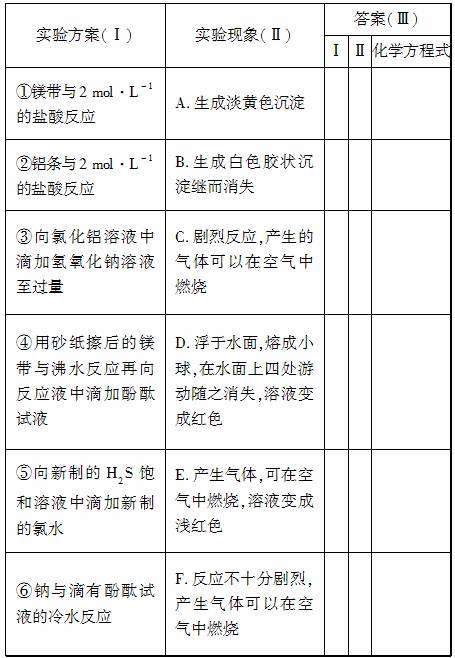
(1)该同学的实验目的是________________________________。
(2)从实验结果可以得出的结论是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于蛋白质的叙述错误的是( )
A.浓HNO3溅在皮肤上,使皮肤呈黄色,是由于浓HNO3和蛋白质发生了颜色反应
B.蛋白质溶液中加入饱和(NH4)2SO4溶液,蛋白质析出,再加水也不溶解
C.蛋白质水解的最终产物是氨基酸
D.高温灭菌的原理是加热后使蛋白质变性,从而使细菌死亡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com