
【题目】人体尿液中可以分离出具有生长素效应的化学物质——吲哚乙酸,吲哚乙酸的结构简式如图所示。下列有关说法正确的是( )
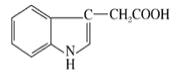
A.分子中含有2种官能团且有两性
B.1mol吲哚乙酸与足量氢气发生反应,最多消耗5molH2.
C.吲哚乙酸苯环上的二氯代物共有六种
D.分子中含一个手性碳原子
科目:高中化学 来源: 题型:
【题目】有几种芳香族化合物的结构如下所示,
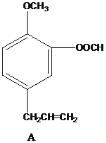
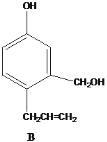
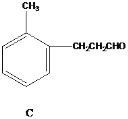

请回答下列问题:
(1)写出A中无氧官能团的名称____,写出C与银氨溶液反应的化学反应方程式___________ 。
(2)能发生银镜反应的物质有____(填序号)。
(3)D的同分异构体有多种,请写出核磁共振氢谱峰面积之比为3:2:2:1的结构简式___(写出1种即可)。
(4)B与足量浓溴水反应,所得产物的结构简式为 ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经研究发现白蚁信息素有:![]() (2,4-二甲基-1-庚烯),
(2,4-二甲基-1-庚烯),![]() (3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)8CH==CH—CH==CH(CH2)8CH3。下列说法不正确的是
(3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)8CH==CH—CH==CH(CH2)8CH3。下列说法不正确的是
A.2,4-二甲基1庚烯的分子式为C9H18
B.2,4-二甲基-1-庚烯与3,7-二甲基-1-辛烯互为同系物
C.以上三种信息素均能使溴的四氯化碳溶液褪色
D.1 mol家蚕的性信息素与1 mol Br2加成,产物只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)又称联氨,是火箭常用的高能燃料,常温下为液体,其球棍分子模型如图所示。肼能与双氧水发生反应 N2H4+2H2O2=N2+4H2O,用 NA表示阿伏加德罗常数的值。下列说法正确的是
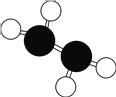
A.N2H4属于共价化合物,分子中只含有极性共价键
B.标准状况下,22.4 L N2H4中含有的原子总数为 6NA
C.标准状况下,3.2 g N2H4中含有共价键的总数为 0.6NA
D.若生成 3.6g H2O,则上述反应转移电子的数目为 0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼化钒(VB2)空气电池是目前储电能力最高的电池,电池示意图如图,该电池工作时发生的反应为:4VB2+11O2=4B2O3+2V2O5。下列说法不正确的是( )
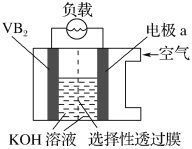
A.电极a为电池正极
B.电池工作过程中,电极a附近区域pH减小
C.图中选择性透过膜为阴离子透过膜
D.VB2极发生的电极反应为:2VB2+22OH--22e-=V2O5+2B2O3+11H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物的转化对工农业生产及环境保护有重要的意义。
(1)下面是氮的氧化物在几种不同情况下的转化:
①已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6kJ·mol-1
2SO3(g) ΔH=-196.6kJ·mol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0kJ·mol-1
2NO2(g) ΔH=-113.0kJ·mol-1
则SO2气体与NO2气体反应生成SO3气体和NO气体的热化学方程式为___。
②a.向绝热恒容密闭容器中通入SO2和NO2,一定条件下使其反应达到平衡,正反应速率随时间变化的示意图如图1所示。反应在c点___(填“达到”或“未到”)平衡状态。
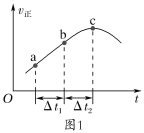
b.开始时,分别在该容器中加入Ⅰ:2molSO2(g)和2molNO2(g);Ⅱ:2molSO3(g)和2molNO(g)。则反应达到平衡时,平衡常数:Ⅰ__(填“>”“=”或“<”)Ⅱ。
(2)常温时向浓度为0.1mol·L-1体积为V L的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸体积的变化曲线如图2所示,d点处两种溶液恰好完全反应。根据图2回答下列问题:
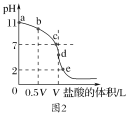
①b、c、d三点对应的溶液中,水电离的c(OH-)由大到小的顺序为____。
②滴定时,由b点到c点的过程中,下列各选项中数值保持不变的有___。
a.![]() b.
b.![]()
c.![]() d.
d.![]()
③该温度时氨水的电离平衡常数K=___。
(3)氮的氧化物易污染环境,可用氢氧化钠溶液吸收。发生的反应为:
2NaOH+NO+NO2=2NaNO2+H2O
2NaOH+2NO2=NaNO3+NaNO2+H2O
将反应混合液和氢氧化钠溶液分别加到如图3所示的电解槽中进行电解,A室产生N2。
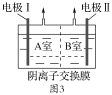
①电极Ⅱ是__极,B室产生的气体是___。
②A室NO2-发生的电极反应是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是“国际化学元素周期表年”。1869年门捷列夫把当时已知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下所示。下列说法错误的是

A.甲位于现行元素周期表第四周期第ⅢA族
B.原子半径比较:甲>乙>Si
C.原子序数:甲-Ca=1
D.推测乙的单质可以用作半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中各组物质之间不能通过一步反应实现如图的是( )
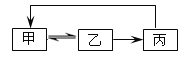
甲 | 乙 | 丙 | |
A | NaHCO3 | Na2CO3 | NaCl |
B | SiO2 | H2SiO3 | Na2SiO3 |
C | Cl2 | HCl | CuCl2 |
D | AlCl3 | Al(OH)3 | Al2O3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍钴锰酸锂电池是一种高功率动力电池。采用废旧锂离子电池回收工艺制备镍钴锰酸锂三元正极材料(铝电极表面涂有LiNi1-x-yCoxMnyO2)的工艺流程如图所示:
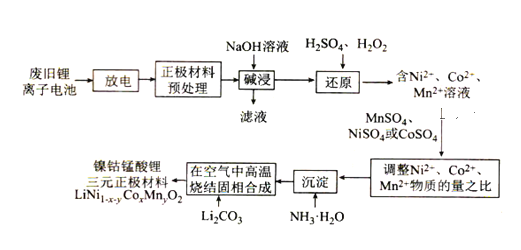
回答下列问题
(1)废旧锂离子电池拆解前进行“放电处理”有利于锂在正极的回收,其原因是___。
(2)能够提高“碱浸”效率的方法有___(至少写两种)。
(3)“碱浸”过程中,铝溶解,在该反应中每产生1mol非极性共价键放出133.3kJ的热量,请写出该反应的热化学方程式___。
(4)实验室模拟“碱浸”后过滤的操作,过滤后需洗涤,简述洗涤的操作过程:___。
(5)LiCoO2参与“还原”反应的离子方程式为___。在该反应中H2O2做___(氧化剂,还原剂)1molH2O2参与反应转移__ NA个电子
(6)溶液温度和浸渍时间对钴的浸出率影响如图所示,则浸出过程的最佳条件是___。
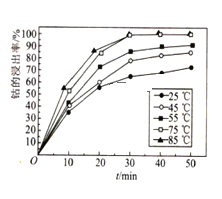
(7)已知溶液中Co2+的浓度为1.0mol·L-1,缓慢通入氨气,使其产生Co(OH)2沉淀,则Co2+沉淀完全时溶液的最小pH为____(已知:离子沉淀完全时c(Co2+)≤1.0×10-5mol·L-1,Ksp[Co(OH)2]=4.0×10-15,1g5=0.7,1g2=0.3,溶液体积变化忽略不计)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com