
向H2O2溶液中加入适量稀硫酸酸化的硫酸亚铁溶液,依次观察到如下现象:①反应刚开始,仅有少量气泡产生;②反应片刻后,有大量气泡产生;③试管底部最终出现红褐色沉淀。下列判断正确的是
A.①中仅发生一个反应 B.Fe3+能催化H2O2的分解
C.反应过程中溶液pH不断减小 D.FeSO4与等物质的量的H2O2恰好反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
铅酸蓄电池是目前应用普遍的化学电池,新型液流式铅酸蓄电池以可溶的甲基磺酸铅为电解质,电池总反应:Pb+PbO2+4H+ 2Pb2++2H2O
2Pb2++2H2O
下列有关新型液流式铅酸蓄电池的说法不正确的是( )
A.放电时,蓄电池由化学能转化为电能
B.充放电时,溶液的导电能力变化不大
C.放电时的负极反应式为Pb-2e-===Pb2+
D.充电时的阳极反应式为Pb2++4OH-+2e-===PbO2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,在一密闭容器中将1.0 mol/L N2与3.0 mol/L H2合成氨,反应到2s时测得
NH3的浓度为0.8 mol/L,用N2浓度的变化量来表示该反应速率时,该反应的反应速率为
A、0.2 mol/(L·s) B、0.4 mol/(L·s) C、0.6 mol/(L·s) D、0.8 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是 ( )。
A.NH3、CO、CO2都是极性分子
B.CH4、CCl4都是含有极性键的非极性分子
C.HF、HCl、HBr、HI的稳定性依次增强
D.CS2、H2O、C2H2都是直线形分子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列过程属于物理变化的是
A.平行光照射胶体产生丁达尔现象 B.紫外线照射下,液态蛋白质凝固
C.电解质溶液导电过程 D.铁遇到冷的浓硝酸溶液发生钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
Fe、C、N、O、H可以组成多种物质。回答以下问题:
(1)基态铁原子中,未成对电子数有 个。
(2)铁单质在一定条件下可与CO反应生成配位化合物——羰基
铁[Fe(CO)5],其结构如右图。已知CO分子与N2分子结构相
似,分子中C、O原子均能提供孤电子对形成配位键。
①CO分子中σ键与π键数目之比为 ;
②从电负性角度分析,Fe(CO)5中与Fe形成配位键的是 (填“碳”或“氧”)原子。
 ③与羰基铁分子的极性相似的分子是 。
③与羰基铁分子的极性相似的分子是 。
A.SO2 B.CS2 C.BF3 D.PCl3
(3)CH4、H2O分子的键角分别为a、b。则a b
(填>、=或<),原因是 。
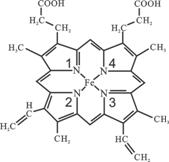
(4)血红素分子结构如右图所示。
①血红素分子间存在的作用力有 (填名称);
②与Fe通过配位键结合的氮原子的编号是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于元素周期表和元素周期律的说 法正确的是 ( )
法正确的是 ( )
A.Li、Na、K元素的原子核外电子层数随着核电荷数的增加而减少
B.因为K比Na容易失去电子,所以K比Na的还原性强
C.第二周期元素从Li到F,非金属性逐渐减弱
D.O与S为同主族元素,且O比S的非金属性弱
查看答案和解析>>
科目:高中化学 来源: 题型:
在10 L的密闭容器中进行反应N2(g) + 3H2(g) 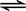 2NH3(g),2 min末N2的物质的量由20 mol减小到8 mol,则2 min末N2的反应速率为
2NH3(g),2 min末N2的物质的量由20 mol减小到8 mol,则2 min末N2的反应速率为
A.1.2 mol/(L·min) B.1 mol/(L·min)
C.0.6 mol/(L·min) D.0.4 mol/(L·min)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com