
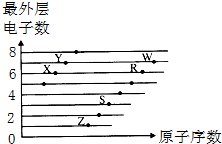
| A. | X的某种单质是一种新型自来水消毒剂 | |
| B. | 简单离子半径:W->R2->X2->S3+ | |
| C. | R、Z不可能形成离子化合物 | |
| D. | 字母所代表的元素中最高价氧化物的水化物酸性最强的是Y |
分析 都是短周期元素,由最外层电子数与原子序数关系可知,X、Y处于第二正确,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、S、R、W处于第三周期,最外层电子数分别为1、3、6、7,故Z为Na元素、S为Al、R为S元素、W为Cl元素,据此进行解答.
解答 解:都是短周期元素,由最外层电子数与原子序数关系可知,X、Y处于第二正确,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、S、R、W处于第三周期,最外层电子数分别为1、3、6、7,故Z为Na元素、S为Al、R为S元素、W为Cl元素.
A.臭氧具有杀菌消毒作用,是一种新型自来水消毒剂,故A正确;
B.电子层结构相同的离子,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径:S2->Cl->O2->Al3+,故B错误;
C.R、Z能形成Na2S,属于离子化合物,故C错误;
D.F元素没有最高价含氧酸,最高价氧化物的水化物酸性最强的是高氯酸(Y元素的最高价含氧酸),故D错误,
故选A.
点评 本题考查结构性质位置关系、元素周期律等,难度不大,根据最外层电子数及原子序数的关系确定元素是解题的关键,注意整体把握元素周期表的结构.


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:选择题
| A. | NH4+、H+、NO3-、HCO3- | B. | K+、Na+、HCO3-、OH- | ||
| C. | Na+、Ba2+、SO32-、Cl- | D. | Na+、CH3COO-、CO32-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 盐酸 | 50mL | 50mL | 50mL |
| m(混合物) | 9.2g | 14.2g | 27.6g |
| V(CO2)(标准状况) | 2.24L | 3.36L | 3.36L |
| A. | 盐酸的物质的量浓度为3.0 mol/L | |
| B. | 当混合物质量为9.2 g时,50 mL盐酸恰好完全反应 | |
| C. | 混合物中NaHCO3、KHCO3的物质的量之比为1:2 | |
| D. | 混合物中NaHCO3的质量分数为45.7% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 实验 | 操作 |
| A | 钠与水反应 | 用镊子从煤油中去除金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
| B | 配制一定浓度的碳酸钠溶液1000mL | 准确称取碳酸的固体,放入到1000mL的容量瓶中,加水溶解,振荡摇匀、定容 |
| C | 排除碱式滴定管尖嘴部分的气泡 | 将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出 |
| D | 去除分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出至截面上,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端放出 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
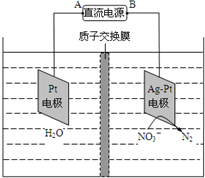 电化学降解NO3-的原理如图所示,若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(△m左-△m右)为a克,则a值为( )
电化学降解NO3-的原理如图所示,若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(△m左-△m右)为a克,则a值为( )| A. | 14.4 | B. | 10.4 | C. | 12.4 | D. | 14.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑤ | B. | ③⑤⑥ | C. | ①②④⑦ | D. | ②⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 H、C、N、F、Al、Ca、Ni、Cu是中学阶段常见的元素,回答下面几个小题
H、C、N、F、Al、Ca、Ni、Cu是中学阶段常见的元素,回答下面几个小题查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com