
25℃时,物质的量浓度相等的CH3COOH和NH3·H2O的稀溶液,两者pH之和为14。
有一种并不常用的酸碱指示剂,是中性红和次甲基蓝在酒精中的混合溶液,称为“中性红-次甲基蓝混合指示剂”,它恰好能在pH=7时在溶液中呈紫蓝色,在酸性溶液中呈紫色,在碱性溶液中呈绿色。
(1)已知0.05mol·L-1NH4Cl溶液的pH=5.3,试推断0.05 mol·L-1CH3COONa溶液的pH为____。
(2)用NaOH标准溶液(准确浓度接近0.1 mol·L-1)测定待测的CH3COOH溶液浓度的实验方案中,试回答下列问题:
①中性红-次甲基蓝混合指示剂________(填“能”或“不能”)用于本实验的滴定?说明理由
________________________________________________________________________。
②常用的酸碱指示剂中__________适用于本实验的滴定。判断滴定终点的方法是________
____________________________________________________________________。
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:阅读理解
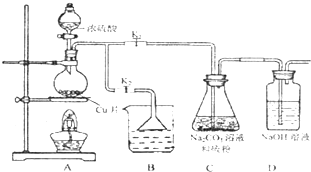 硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.2- 4 |
2- 7 |
| 编号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准溶液的体积/mL | 18.02 | 17.98 | 18.00 | 20.03 |
2- 7 |
2- 3 |
2- 6 |
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022
①称取n g草酸晶体配制100.00mL的水溶液 ②取25.00mL所配制的草酸溶液置于 锥形瓶中,加稀硫酸,用浓度为amol/L的KMnO4溶液滴定,所发生的反应为:
2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O,反应生成的 MnSO4在水溶液中基本无色,试回答下列问题:
(1)实验中不需要的仪器是________(填序号),还缺少的仪器有________(填名称)。
a.托盘天平(带砝码、镊子);b.滴定管;c.100 mL,量筒;d.100mL容量瓶;e.烧杯; f.漏斗;g.锥形瓶;h.玻璃棒;i.药匙;j.烧瓶。
(2)实验中。KMnO4溶液应装在________式滴定管中,因为________。
(3)滴定过程中用去V mL amol/L的KMnO4溶液,则所配制的草酸的物质的量浓 度为mol/L,由此可计算x的值为________。
(4)若滴定终点读数时目光俯视,则计算x值可能________(填偏大、偏小、无影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:022
草酸晶体的组成可表示为H2C2O4·xH2O,为了测定x值,进行下述实验:
①称取n g草酸晶体配制100.00mL的水溶液 ②取25.00mL所配制的草酸溶液置于 锥形瓶中,加稀硫酸,用浓度为amol/L的KMnO4溶液滴定,所发生的反应为:
2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O,反应生成的 MnSO4在水溶液中基本无色,试回答下列问题:
(1)实验中不需要的仪器是________(填序号),还缺少的仪器有________(填名称)。
a.托盘天平(带砝码、镊子);b.滴定管;c.100 mL,量筒;d.100mL容量瓶;e.烧杯; f.漏斗;g.锥形瓶;h.玻璃棒;i.药匙;j.烧瓶。
(2)实验中。KMnO4溶液应装在________式滴定管中,因为________。
(3)滴定过程中用去V mL amol/L的KMnO4溶液,则所配制的草酸的物质的量浓 度为mol/L,由此可计算x的值为________。
(4)若滴定终点读数时目光俯视,则计算x值可能________(填偏大、偏小、无影响)。
查看答案和解析>>
科目:高中化学 来源:北京市石景山区2006-2007学年度高三年级第一学期期末统一考试、化学 题型:058
| |||||||||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com