
| A. | 有单质生成的分解反应一定是氧化还原反应 | |
| B. | 某元素从化合态变为游离态时,该元素一定被还原 | |
| C. | 氧化剂被氧化,还原剂被还原 | |
| D. | 没有氧元素参加的反应一定不是氧化还原反应 |
分析 A.有单质生成的分解反应一定有电子转移;
B.某元素从化合态转化为游离态,可能失电子也可能得电子;
C.氧化剂被还原,还原剂被氧化;
D.只要有电子转移的反应就一定是氧化还原反应,但不一定有O元素参加反应.
解答 解:A.有单质生成的分解反应一定有电子转移,所以一定是氧化还原反应,故A正确;
B.某元素从化合态转化为游离态,可能失电子也可能得电子,如Cl-→Cl2时氯离子被氧化,Cu 2+→Cu时铜离子被还原,故B错误;
C.氧化剂具有氧化性,所以在反应中氧化剂被还原,还原剂具有还原性,所以在反应中还原剂被氧化,故C错误;
D.只要有电子转移的反应就一定是氧化还原反应,但不一定有O元素参加反应,如H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl,故D错误;
故选A.
点评 本题考查氧化还原反应,为高频考点,明确氧化还原反应本质及特征是解本题关键,知道氧化性、还原性与元素化合价变化关系,易错选项是D.


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:选择题
| A. | 8.2L | B. | 11.5L | C. | 15.7L | D. | 16.8L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
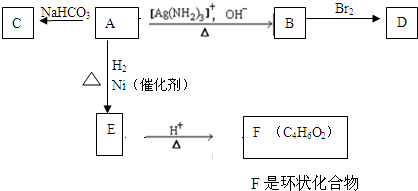
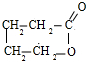 .由E生成F的反应类型是酯化反应.
.由E生成F的反应类型是酯化反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,在pH=7的醋酸钠和醋酸混合溶液中,c(CH3COO-)>c(Na+) | |
| B. | 稀释醋酸溶液,溶液中所有离子的浓度均降低 | |
| C. | 在pH=5的氯化钠和稀硝酸的混合溶液中,c(Na+)=c(Cl-) | |
| D. | 在0.1 mol•L-1的硫化钠溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
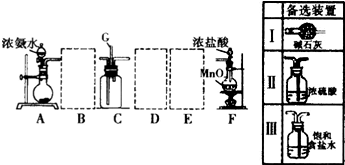
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
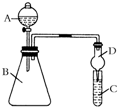 某同学为验证元素周期表中元素性质的递变规律,利用如图装置可验证同主族非金属性的变化规律.设计了如下系列实验.
某同学为验证元素周期表中元素性质的递变规律,利用如图装置可验证同主族非金属性的变化规律.设计了如下系列实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属镁能在CO2中燃烧,则金属钠也能在CO2中燃烧 | |
| B. | 金属钠与水反应产生NaOH和H2,则金属铜与水反应也能产生Cu(OH)2和H2 | |
| C. | Cl2+H2O?HCl+HClO是氧化还原反应,则ICl+H2O?HCl+HIO也是氧化原反应 | |
| D. | CO2与H2O反应生成H2CO3,则SiO2与H2O反应也可以生成H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com