
| A. | 将Cl2通入H2O中:Cl2+H2O═2H++Cl-+ClO- | |
| B. | NaOH溶液中加入Al粉:2Al+4OH-═2AlO2-+2H2O | |
| C. | 氯化亚铁溶液中加入新制氯水:Cl2+Fe2+═Fe3++2Cl- | |
| D. | NaHCO3溶液与盐酸的反应:HCO3-+H+═CO2↑+H2O |
分析 A.次氯酸是弱电解质,应写化学式;
B.注意该反应中水是反应物,铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,方程式左右电荷也不守恒;
C.氯化亚铁与氯气反应生成氯化铁,方程式左右电荷不守恒;
D.NaHCO3溶液与盐酸的反应生成氯化钠、水、二氧化碳.
解答 解:A.氯气与水反应生成的次氯酸是弱电解质,离子方程式为:Cl2+H2O═H++Cl-+HClO,故A错误;
B.铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,离子反应方程式为:2Al+2OH-+2H2O=+2AlO2-+3H2↑,故B错误;
C.氯化亚铁与氯气反应生成氯化铁,反应的离子方程式为:Cl2+2Fe2+=2Cl-+2Fe3+,故C错误;
D.NaHCO3溶液与盐酸的反应生成氯化钠、水、二氧化碳,反应的离子方程式为:HCO3-+H+═CO2↑+H2O,故D正确;
故选D.
点评 本题考查了离子方程式的正误判断,解题时注意从化学式、离子符号、电荷守恒、是否符合反应实际的角度分析离子方程式的书写是否正确,题目难度不大.


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
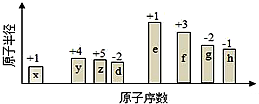 随原子序数的递增,八种短周期元素(用字母表示)原子半径的相对大小、最高正价或最低负价的变化如图所示.根据判断出的元素回答下列问题:
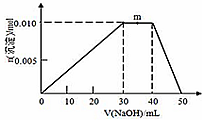
随原子序数的递增,八种短周期元素(用字母表示)原子半径的相对大小、最高正价或最低负价的变化如图所示.根据判断出的元素回答下列问题: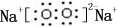 ;B是常见的液态化合物,其稀溶液易被催化分解,可使用的催化剂为AB.(填序号)
;B是常见的液态化合物,其稀溶液易被催化分解,可使用的催化剂为AB.(填序号)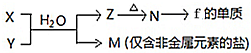
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,100g 17%H2O2水溶液中含氧原子总数为NA | |
| B. | 常温常压下,2.8g N2气体分子中所含的共用电子对数目为0.3NA | |
| C. | 0.2mol/L的NaCl溶液中含有的Cl-数是0.2NA | |
| D. | 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 乙醇 | B. | 乙醚 | C. | 正丙醇 | D. | 丙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁粉与氯化铁恰好完全反应,Cl-基本保持不变 | |
| B. | 往溶液中滴入无色KSCN溶液,溶液变红色 | |
| C. | 氧化产物和还原产物的物质的量之比为1:2 | |
| D. | 反应后溶液中Fe2+ 离子的浓度为 4 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小苏打--Na2CO3 | B. | 熟石灰--Ca (OH)2 | C. | 漂白粉-Ca(ClO)2 | D. | 氯水--Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com