
【题目】下列实验操作中,所用仪器合理的是( )
A. 在坩埚中放入NaCl溶液,加热、蒸发得到NaCl晶体
B. 用10 mL的量筒量取9.20 mL的盐酸
C. 用托盘天平称取5.00 g NaCl
D. 用500 mL容量瓶配制450 mL 0.1 mol·L-1的盐酸
科目:高中化学 来源: 题型:
【题目】资料显示,可用次氯酸钠处理废水中的氨氮(NH3),使其转化为氮气除去,其主要反应如下: ①NH3(aq)+HClO(aq)═NH2Cl(aq)+H2O(l)
②2NH2Cl(aq)+HClO(aq)═N2(g)+H2O(l)+3HCl(aq)
(1)在其他条件不变的情况下,向一定量废水中逐滴滴加次氯酸钠溶液,氨氮去除率随 ![]() 的变化曲线如图1:
的变化曲线如图1: 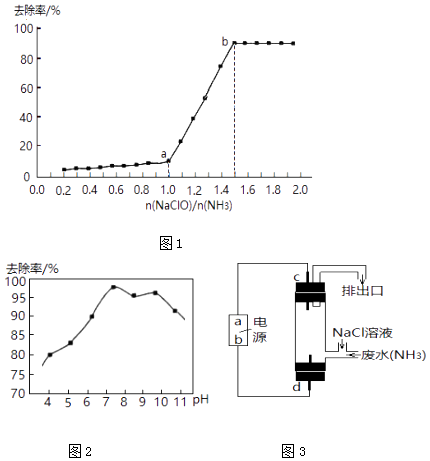
Ⅰ.物质NH2Cl中氮元素的化合价是 .
Ⅱ.a﹣b点间,溶液中氨氮去除率迅速提高的原因是 .
(2)Ⅰ.反应①②中HClO 的来源用化学用语解释是 . Ⅱ.实验测得,废水中pH与氨氮去除率如图2所示:
pH较高时,氨氮去除率下降的原因是 .
pH较低时,氨氮去除率也下降,可能的原因是 .
(3)运用上述原理去除废水中的氨氮,可结合图3所示的电解法. Ⅰ.a极为 .
Ⅱ.d极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇在生活中用途较多,下列关于乙醇的说法正确的是
A. 能与Na反应
B. 是食醋的主要成分
C. 能使红色石蕊试纸变蓝
D. 能与饱和Na2CO3溶液反应产生H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在酸性条件下有以下反应关系:KBrO3能将KI氧化成I2; Br2能将I﹣氧化为I2 . IO3﹣也能将Br﹣氧化为Br2 , 其本身被还原为I2 . 现向含有1mol KI的硫酸溶液中加入含amol KBrO3溶液,a的取值不同,所得产物也不同.下列判断正确是( )
编号 | a的取值范围 | 产物的化学式(或离子符号) |
① | a≤ | I2Br﹣ |
② |
| I2Br﹣Br2 |
③ |
| I2 IO3﹣ Br2 |
④ | a≥ | IO3﹣ Br2 |
A.①③④
B.②③④
C.①②③④
D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用100ml 0.5molL﹣1Na2CO3溶液配制Na+浓度为0.20molL﹣1的溶液,下列操作正确的是( )
A.将该Na2CO3 溶液转移至250ml容量瓶中,加蒸馏水稀释至刻度线,摇匀
B.将该Na2CO3 溶液转移至250ml烧杯中,用量筒量取150ml蒸馏水加入,搅拌
C.将该Na2CO3 溶液转移至250ml烧杯中,用量筒量取400ml蒸馏水加入,搅拌
D.将该Na2CO3 溶液转移至500ml容量瓶中,加蒸馏水稀释至刻度线,摇匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是我国化学家近年来合成的两种聚乙炔衍生物分子的结构式. 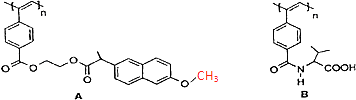
下列说法正确的是( )
A.A和B均能在一定条件下水解,且水解均生成两种产物
B.A水解生成的高分子化合物中所有碳原子一定共面
C.A和B的链节中均含有2个以上手性碳原子
D.1molA和B各与热碱液反应,均最多消耗2n mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国对中药中重金属元素和有毒元素的含量等各项指标检查是非常严格的.下面是分析实验室对中草药中可能的残余有毒元素As的检验方法和步骤(As在中草药中主要以As2O3的形式存在):
①取1000g中草药样品进行前期处理制得待测溶液,此时样品中可能含有的As元素将转化为H3AsO3;
②将待测溶液转移到250mL锥形瓶中,并加入2﹣3滴0.2%的淀粉溶液;
③用0.001mol/L标准碘溶液滴定待测溶液至终点,消耗20.00mL标准I2溶液,发生的反应为:H3AsO3+I2+H2O→H3AsO4+I﹣+H+(未配平)
试回答下列问题:
(1)简述如何对中草药样品进行前期处理制得待测溶液? .
(2)配平离子反应方程式:H3AsO3+I2+H2O﹣H3AsO4+I﹣+H+
(3)如何判断滴定到达终点? .
(4)我国《药用植物及制剂进出口绿色行业标准》中规定:绿色中药的砷含量不能超过2.000mg/kg,试计算该草药样品中砷含量为mg/kg,则该草药样品(填“合格”或“不合格”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A,B,C,D是中学化学的常见物质,且A,B,C均含有同一种元素.在一定条件下,它们之间的相互转化关系如图所示(反应中生成的H2O已略去).请回答下列问题: ![]()
(1)若A是一种可用于自来水消毒的黄绿色气体,D是生活中常用的金属单质,则C的化学式为;写出A与C反应的离子方程式 .
(2)若A是一种常见的强碱,C常用于糕点发酵,则反应①的离子方程式是 .
(3)若A是一种碱性气体,常用作制冷剂,B,D是空气中的主要成分,则C的化学式为 .
(4)若A是一种无色、有臭鸡蛋气味的气体,C是导致酸雨的主要气体,则反应③的方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 1 molNaCl约含有6.02×1023个NaCl分子
B. 1 mol Ne中含有约6.02×1024个电子
C. 1 mol水中含2 mol氢和1 mol氧
D. 标准状况下,11.2L CCl4所含分子数为0.5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com