
| A. | (CH3)3COH的名称:2,2二甲基乙醇 | B. | 乙醛的结构式:CH3CHO | ||
| C. | CH4分子的比例模型: | D. | 丙烯分子的结构简式为 CH3CHCH2 |
分析 A、醇在命名时,要选含官能团的最长的碳链为主链,从离官能团近的一端给主链上的碳原子进行编号,并标注出官能团的位置;
B、结构式是用一条短线代替一对共用电子对所得到的式子;
C、比例模型主要体现出分子中各原子相对体积大小,据此判断甲烷的比例模型;
D、烯烃的结构简式中碳碳双键不能省略.
解答 解:A、醇在命名时,要选含官能团的最长的碳链为主链,从离官能团近的一端给主链上的碳原子进行编号,并标注出官能团的位置,故(CH3)3COH的主链上有3个碳原子,在2号碳原子上有一个甲基和一个-OH,故名称是2-甲基-2-丙醇,故A错误;
B、结构式是用一条短线代替一对共用电子对所得到的式子,故乙醛的结构式为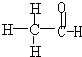 ,故C错误;
,故C错误;
C、甲烷为正四面体结构,碳原子半径大于氢离子,则甲烷的比例模型为: ,故C正确;
,故C正确;
D、烯烃的结构简式中碳碳双键不能省略,故丙烯分子的结构简式为 CH3CH=CH2,故D错误.
故选C.
点评 本题考查常用化学用语的表示方法判断,题目难度中等,涉及球棍模型、结构简式、结构式等知识,注意掌握结构简式、结构式的区别,明确常见化学用语的书写原则为解答关键.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案科目:高中化学 来源: 题型:选择题
| A. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | B. | 第一电离能:Na<Mg<Al | ||
| C. | 电负性:Na<Mg<Al | D. | 还原性:Na>Mg>Al |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
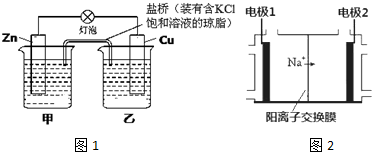
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4、Cl2 | B. | CH3CH3、HCl | C. | CH≡CH、HCl | D. | CH2=CH2、HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(g)△H=-1367.0 kJ/mol(燃烧热) | |
| B. | S(s)+O2(g)=SO2(g)△H=-269.8kJ/mol (反应热) | |
| C. | NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(1)△H=+57.3kJ/mol(中和热) | |
| D. | 2NO2=O2+2NO△H=+116.2kJ/mol (反应热) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.3g钠与水反应失去的电子数目为0.2NA | |
| B. | 20℃、101KPa时,5.6L NH3 所含的原子数目为NA | |
| C. | 10℃、101KPa时,16g CH4 所含有的电子数为10NA | |
| D. | 1mol NaCl固体溶于1L水所得的溶液中NaCl的物质的量浓度为1 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com