
已知: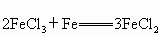 ,
,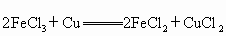 ,向含有a mol
,向含有a mol 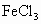 和b mol
和b mol 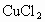 的溶液中投入含c mol Fe和d mol Cu的混合物.若充分反应后,仍有固体存在,请分析固体的可能成分及溶液中离子情况,(1)按要求填入下表(不考虑
的溶液中投入含c mol Fe和d mol Cu的混合物.若充分反应后,仍有固体存在,请分析固体的可能成分及溶液中离子情况,(1)按要求填入下表(不考虑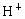 、
、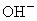 ,空格若无内容即填“无”);(2)若只投入过量的铁粉末,充分反应后,固体质量不变,则
,空格若无内容即填“无”);(2)若只投入过量的铁粉末,充分反应后,固体质量不变,则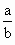 =_________.
=_________.

 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
 课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y 都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.试回答下列问题:
课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y 都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.试回答下列问题:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
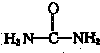 )与NO2-在酸性条件下反应生成两种无毒气体.该反应中生成16.8L(已折算为标准状况)混合气体时,消耗尿素的质量为
)与NO2-在酸性条件下反应生成两种无毒气体.该反应中生成16.8L(已折算为标准状况)混合气体时,消耗尿素的质量为查看答案和解析>>
科目:高中化学 来源: 题型:022
已知: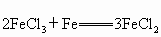 ,
,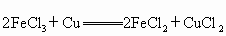 ,向含有a mol
,向含有a mol 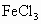 和b mol
和b mol 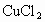 的溶液中投入含c mol Fe和d mol Cu的混合物.若充分反应后,仍有固体存在,请分析固体的可能成分及溶液中离子情况,(1)按要求填入下表(不考虑
的溶液中投入含c mol Fe和d mol Cu的混合物.若充分反应后,仍有固体存在,请分析固体的可能成分及溶液中离子情况,(1)按要求填入下表(不考虑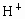 、
、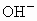 ,空格若无内容即填“无”);(2)若只投入过量的铁粉末,充分反应后,固体质量不变,则
,空格若无内容即填“无”);(2)若只投入过量的铁粉末,充分反应后,固体质量不变,则 =_________.
=_________.

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com