
根据原子结构及元素周期律的知识,下列推断正确的是
A.同主族元素含氧酸的酸性随核电荷数的增加而减弱
B.核外电子排布相同的微粒化学性质也相同
C.Cl‾、S2‾、Ca2+、K+半径逐渐减小 D.35Cl2与37Cl2得电子能力相同
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下图表示元素周期表中前4周期的一部分元素,下列有关叙述正确的是 ( )
A.b、c、e三种元素的原子半径大小关系:e>c>b
B.六种元素分别形成的单质晶体中,e的熔、沸点最高
C.b的氢化物沸点比f的氢化物沸点低
D.c元素除0价外,只有一种化合价

查看答案和解析>>
科目:高中化学 来源: 题型:
两种气态烃组成的混合物0.1 mol 完全燃烧得0.16 molCO2和3.6g水。下列说法正确
的是 ( )
A.一定有甲烷 B.一定有甲烷和乙烯 C.一定有乙烷 D.一定有乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
空气吹出法工艺,是目前“海水提溴”的最主要方法之一.其工艺流程如下: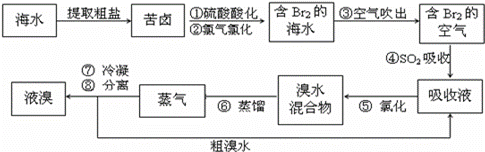
(1)溴在周期表中位于 周期 族.
(2)步骤①中用硫酸酸化可提高Cl2的利用率,理由是 .
(3)步骤④利用了SO2的还原性,反应的离子方程式为 ﹣ .
(4)步骤⑥的蒸馏过程中,温度应控制在80﹣90℃.温度过高或过低都不利于生产,请解释原因: .
(5)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离.分离仪器的名称是 .
(6)步骤①、②之后并未直接用“含Br2的海水”进行蒸馏得到液溴,而是经过“空气吹出”、“SO2吸收”、“氯化”后再蒸馏,这样操作的意义是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,10 mL 0.40 mol/L H2O2溶液发生催化分解,不同时刻测得生成O2的体积(已折算为标准状况)如下表。
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6 min的平衡反应速率:v(H2O2)≈3.3×10-2 mol/(L·min)
B.6~10 min的平衡反应速率:v(H2O2)<3.3×10-2 mol/(L·min)
C.反应到6 min时,c(H2O2)=0.30 mol/L
D.反应到6 min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源: 题型:
加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯,用下图所示装置探究废旧塑料的再利用。下列叙述不正确的是
A.丙烯分子中共用电子对数为10
B.装置B的试管中可收集到芳香烃
C.装置C中的试剂可吸收烯烃以制取卤代烃
D.最后收集的气体可做燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.原子的电子层数越多,原子半径越大
B.同族元素相差的原子序数可能为16、26、36、46
C.ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物
D.卤族元素的单质均有氧化性,最高正价都是+7
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解下列足量的溶液,一段时间后,再加入一定量的另一物质(括号内)后,溶液能与原来溶液浓度一样的是 ( )
A.CuCl2(CuCl2溶液) B.AgNO3(Ag2O) C.NaCl(HCl溶液) D.CuSO4(Cu(OH)2)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com