
【题目】下列说法正确的是( )
A.酯的水解反应和酯化反应都属于取代反应
B.乙烯能使溴水褪色,发生氧化反应
C.乙醇不能被酸性高锰酸钾溶液氧化
D.葡萄糖不能发生银镜反应
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】(1)相对分子质量为84的烃与氢气加成后得到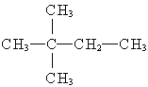 ,该烃的名称为______。
,该烃的名称为______。
(2)某气态烃22.4L(标准状况)与含320 g溴的溴水恰好完全加成,生成物经测定每个碳原子上都有1个溴原子,该烃的结构简式为______。
(3)某烃0.1 mol和0.2 mol HCl完全加成,生成的氯代烷最多还可以与0.6mol氯气反应,则该烃的结构简式为______。
(4)某烃的分子式为C8H10,它不能使溴水褪色,但能使酸性KMnO4溶液褪色。该有机物苯环上的一氯代物有3种,则该烃的结构简式可能为______。
(5)3.4g多元醇A在氧气中完全燃烧时生成CO2和H2O分别为0.125 mol和0.15mol,如将该多元醇的任意一个羟基换成一个卤原子,所得到的卤代物都只有一种,该醇的结构简式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合所学内容,回答下列问题:
Ⅰ.某同学进行影响草酸与酸性高锰酸钾溶液反应速率因素的研究。草酸与酸性高锰酸钾的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。室温下,两支试管分别编号①和②,实验数据如下:
实验序号 | ① | ② |
加入试剂 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 一粒黄豆粒大的MnSO4固体 |
褪色时间/s | 116 | 6 |
试管①中KMnO4溶液褪色的速率开始十分缓慢,一段时间后突然加快。
请回答:
(1)该实验结论是___________________________________________________________。
(2)实验②选用MnSO4固体而不是MnCl2固体的原因是____________________________。
(3)该同学为使实验更加严密,在试管③中做了如下实验,请预测褪色时间约为_____。
实验序号 | ③ |
加入试剂 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 一粒黄豆粒大的Na2SO4固体 |
褪色时间/s |
Ⅱ.滴定法是一种重要的定量分析方法,应用范围很广。某地市场上销售的一种食用精制盐包装袋上有如下部分说明:
产品等级 | 一级 |
配料 | 食盐、碘酸钾(KIO3)、抗结剂 |
碘含量(以I计) | 20~50 mg·kg-1 |
已知:IO3-+5I-+6H+ = 3I2+3H2O,I2+2S2O32- = 2I-+S4O62-某学生拟测定食用精制盐的碘含量,其步骤为
a.准确称取W g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.加入指示剂,逐滴加入物质的量浓度为2.0×10/span>-3 mol·L-1的Na2S2O3溶液10.0 mL,恰好反应完全
(4)c中加入的指示剂可选用_________,恰好完全反应时的现象是_______________。
(5)若操作b在空气中振荡时间过长,则最终测定的测定食用精制盐中的的碘含量会__________(填“偏高”、“偏低”或“没有影响”)。
(6)根据以上实验和包装说明,算得所测食用精制盐的碘含量是(以含W的代数式表示)________mg·kg-1(计算结果保留整数即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近在-100 ℃的低温下合成了一种烃X,红外光谱和核磁共振氢谱表明其分子中的氢原子所处的化学环境没有区别,根据分析,绘制了该分子的球棍模型如图所示。下列说法中不正确的是( )
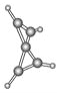
A. 该分子的分子式为C5H4
B. 该分子中碳原子的化学环境有2种
C. 该分子中的氢原子分布在两个相互垂直的平面上
D. 该分子中只有C—C键,没有![]() 键
键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学——选修5:有机化学基础)
合成抗癌新药盐酸埃克替尼的关键中间体G的一种合成路线如下图:
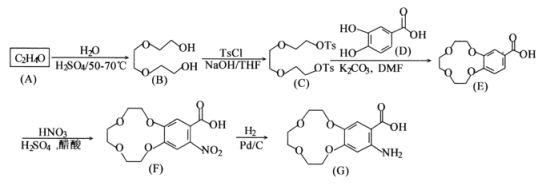
已知:①A分子中只有一种化学环境的氢;
②TsCl为![]()
(1)A的结构简式为__________________。
(2)E的分子式为_____________;G中的含氧官能团的名称有___________。
(3)由E生成F的反应类型是________________。
(4)W是D的同分异构体.W是三取代芳香族化合物,既能发生银镜反应和水解反应,又能与FeC13溶液发生显色反应;1mol W最多可与4mol NaOH反应,W的同分异构体有______种;若W的核磁共振氢谱只有4组峰.则W的结构简式为:_____________。
(5)参照上述合成路线,以(![]() )和邻苯二酚为原料(其它试剂任选),设计制备的
)和邻苯二酚为原料(其它试剂任选),设计制备的 合成路线。_____________________________________
合成路线。_____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A.淀粉和纤维素互为同分异构体。
B.丙酸和甲酸甲酯互为同分异构体
C.乙烯和丙烯互为同系物
D.相差一个或若干个-CH2原子团的有机化合物一定互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取乙酸丁酯的实验装置有如图甲、乙两种装置可供选用。

制备乙酸丁酯所涉及的有关物质的物理性质见下表:
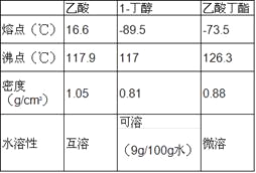
(1)制取乙酸丁酯的装置应选用 ______(填“甲”或“乙”),不选另一种装置的理由是 ______;
(2)该实验生成物中除了主产物乙酸丁酯外,还可能生成的有机副产物有(写出结构简式)__________;
(3)酯化反应是一个可逆反应,为提高1-丁醇的利用率,写出两种可行的方法:
① ______________________________② ____________________________________;
(4)从制备乙酸丁酯所得的混合物中分离、提纯乙酸丁酯时,需要经过多步操作,下列图示的操作中,肯定需要的化学操作是__________________(选填答案编号)。
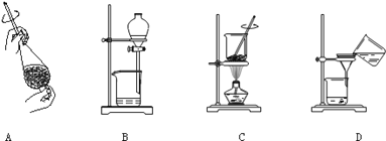
(5)有机物的分离操作中,经常需要使用分液漏斗等仪器.使用分液漏斗前必须 _____,某同学在进行分液操作时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有 ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,若0.1mol/L的一元弱碱的电离度为1%,则下列说法正确的是( )
A.该溶液的pH=11
B.该溶液的pH=3
C.加入等体积0.1mol/LHCl后所得溶液的pH=7
D.加入等体积pH=3的盐酸后所得溶液的pH=7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com