
【题目】碳及其化合物有着重要用途。回答下列问题:
(1)基态碳原子的价层电子排布图为___________。
(2)在CH2=CHCN中,碳原子的杂化方式有___________、___________,所含σ键数目和π键数目之比为___________。
(3)甲烷、水、氨气中C、O、N原子均采用sp3杂化方式,VSEPR模型均为正四面体构型,比较三者键角的大小___________(由大到小,用H一R—H表示),其原因是___________。
(4)C60室温下为紫红色固体,不溶于水,能溶于四氯化碳等非极性溶剂。据此判断C60的晶体类型是___________。
(5)C60晶胞结构如图,C60分子处于顶点和面心。已知:C60晶胞棱长为14.20 (1=10-8cm),则C60的晶体密度为___________g/cm3。
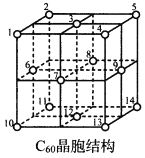
C60体中存在正四面体空隙(例如1、3、6、7四点构成)和正八面体空隙(例如3、6、7、8、9、12六点构成),则平均每一个C60晶胞中有___________个正四面体空隙和4个正八面体空隙。当碱金属元素全部占满所有空隙后,这类C60掺杂物才具有超导性。若用金属铯(Cs)填满所有空隙,距离最近的两个Cs原子间的距离为___________ 。
【答案】 sp、 sp2 2:1 H-C- H>H-N-H>H-O-H C、N、O均为sp3杂化,孤电子对分别为0、1、2,“孤电子对—成键电子对”的斥力大于“成键电子对—成键电子对”的斥力,孤电子对越多斥力越大,键角越小。 分子晶体 1.67 8 7.10
sp、 sp2 2:1 H-C- H>H-N-H>H-O-H C、N、O均为sp3杂化,孤电子对分别为0、1、2,“孤电子对—成键电子对”的斥力大于“成键电子对—成键电子对”的斥力,孤电子对越多斥力越大,键角越小。 分子晶体 1.67 8 7.10
【解析】
(1)基态C原子的核外电子排布式为1s22s22p2,价电子排布式为2s22p2,则价电子排布图为 。
。
(2)CH2=CHCN中,2个C采用sp2杂化、1个C采用sp杂化。![]() 键、π键数目分别为6、3,所含σ键数目和π键数目之比为2:1;答案:sp、sp2;2:1。
键、π键数目分别为6、3,所含σ键数目和π键数目之比为2:1;答案:sp、sp2;2:1。
(3)甲烷、水、氨气中C、O、N原子均采用sp3杂化方式,VSEPR模型均为正四面体构型、理论键角均为10928';但随着孤电子对数目的增多,对成键电子对的斥力越大,实际键角将越小。所以甲烷、水、氨气中C、O、N原子均采用sp3杂化方式,VSEPR模型均为正四面体构型,三者键角的大小为H-C- H>H-N-H>H-O-H;答案:H-C- H>H-N-H>H-O-H;C、N、O均为sp3杂化,孤电子对分别为0、1、2,“孤电子对—成键电子对”的斥力大于“成键电子对—成键电子对”的斥力,孤电子对越多斥力越大,键角越小。
(4)C60是非金属单质晶体,不可能是离子晶体和金属晶体。分子晶体的特点是:熔沸点低,不导电,能溶解在某些溶剂中。而原于晶体一般不溶于其他溶剂。所以C60是分子晶体;答案:分子晶体。
(5)晶胞含有的C60分子数为:8![]() 1/8+6
1/8+6![]() 1/6=4,故密度为4
1/6=4,故密度为4![]() 12
12![]() 60g÷[NA
60g÷[NA![]() (14. 20
(14. 20![]() 10-8cm)3]=1.67g/cm3。正四面体空隙分别是位于1/8晶胞的小立方体的体心位置,共8个(如图
10-8cm)3]=1.67g/cm3。正四面体空隙分别是位于1/8晶胞的小立方体的体心位置,共8个(如图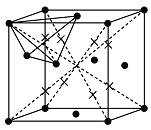 中×),正八面体中心分别位于晶胞体心和晶胞棱中心,1
中×),正八面体中心分别位于晶胞体心和晶胞棱中心,1![]() 1+12
1+12![]() 1/4=4(如图
1/4=4(如图 中)。当Cs原于填入这些空隙后,由这些Cs 原于再次构成立方体,分别位于顶点和体心,故最近的Cs原子为构成的立方体的棱长,等于C60晶胞棱长的1/2 ,即为7.10 。答案:1.67;8;7.10。
中)。当Cs原于填入这些空隙后,由这些Cs 原于再次构成立方体,分别位于顶点和体心,故最近的Cs原子为构成的立方体的棱长,等于C60晶胞棱长的1/2 ,即为7.10 。答案:1.67;8;7.10。


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案科目:高中化学 来源: 题型:
【题目】关于有机物a( )、b(
)、b(![]() )、c(
)、c( )
)
A. a、b、c均能与溴水发生加成反应
B. a、b、c的分子式均为C8H8
C. a的所有原子一定处于同一一平面
D. b的二氯代物有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若实行海水淡化来供应饮用水,下列方法在原理上完全不可行的是( )
A. 加入明矾,使海水的盐分沉淀而淡化
B. 利用太阳能,将海水蒸馏淡化
C. 利用半透膜,采用反渗透法而使海水淡化
D. 将海水通过离子交换树脂,以除去所含的盐分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列五种短周期元素的电离能数据(单位:kJ/mol),回答下面各题。
元素代号 | I1 | I2 | I3 | I4 | I5 |
Q | 800.6 | 2427.1 | 3659.7 | 25025.8 | 32826.7 |
R | 495.8 | 4562 | 6910.3 | 9543 | 13354 |
S | 577.5 | 1816.7 | 2744.8 | 11577 | 14842 |
T | 1402.3 | 2856 | 4578.1 | 7475.0 | 9444.9 |
U | 2080.7 | 3952.3 | 6122 | 9371 | 12177 |
(1)在这五种元素中,最可能处于同一族的两种元素是_________(填元素符号),S元素最可能是_____区元素
(2)基态Q元素原子的价电子排布式是____________。Q和T同周期。化合物QT中T元素的化合价为_______;第一电离能介于Q、T之间的同周期元素有______种。
(3)化合物RT3中化学键类型为_______,RT3的阴离子的几何构型为________。
(4)下列元素中,化学性质和物理性质最像U元素的是_____________
A.硼 B.铍 C.锂 D.氦 E.碳
(5)R的某种氧化物X晶胞结构如图所示,晶胞参数a=0.566 nm,X的化学式为_____;列式并计算晶体X的密度(g·cm-3)_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,属于吸热反应的是( )
①液态水汽化②将胆矾加热变为白色粉末③浓H2SO4稀释 ④KClO3分解制O2⑤生石灰跟水反应生成熟石灰⑥石灰石高温分解⑦铝热反应⑧Ba(OH)2·8H2O与固体NH4Cl混合⑨C+H2O=CO+H2 ⑩Al与盐酸反应
A. ②③④⑥⑦⑧⑨ B. ②④⑥⑧⑨ C. ①②④⑥⑧ D. ②③④⑧⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)从氯化钾溶液中得到氯化钾固体,选择装置________(填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置________。
(2)从碘水中分离出I2,选择装置________,该分离方法的名称为________。
(3)装置A中①的名称是________,进水的方向是从________口进水。装置B在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是____。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:
![]()
![]()
![]()
![]()
![]() ―→
―→![]()
粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④调节溶液的pH等于7 ⑤溶解 ⑥过滤 ⑦蒸发
正确的操作顺序是________(填选项字母)。
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦
c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 标准状况下,22.4L H2含有的原子数为NA
B. 等质量的O2和O3中所含的氧分子数相同
C. 常温常压下,14g N2含有电子数为7NA
D. 等质量的CO与CO2中所含碳原子数之比为7﹕11
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符的是
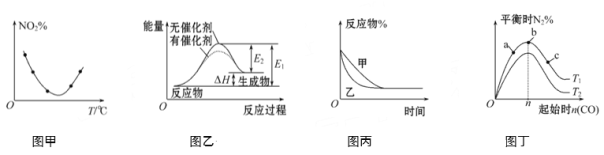
A. 图甲表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)![]() N2O4(g),相同时间后测得NO2含量的曲线,则该反应的ΔH<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的ΔH<0
B. 图乙表示的反应是吸热反应,该图表明催化剂不能改变化学反应的焓变
C. 图丙表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(g)的影响,则P乙>P甲
3C(g)+D(g)的影响,则P乙>P甲
D. 图丁表示反应:4CO(g)+2NO2(g)![]() N2(g)+4CO2(g) ΔH<0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,平衡常数K1>K2
N2(g)+4CO2(g) ΔH<0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,平衡常数K1>K2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com