
| 1 |
| 4 |


科目:高中化学 来源: 题型:
| A、为了减肥,我每天只吃水果、蔬菜 |
| B、食用海产品可防治缺铁性贫血 |
| C、选择食物可调节人体细胞中的酸碱平衡 |
| D、我国应该禁止使用食物防腐剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、温度、容积不变时,通入SO2气体 |
| B、移走一部分NH4HS固体 |
| C、容积不变,充入氨气 |
| D、保持压强不变,充入氮气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
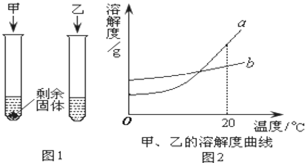 20℃时,向两支试管中加入等质量的甲、乙两种固体物质,分别加入10g水,使其充分溶解,观察到
20℃时,向两支试管中加入等质量的甲、乙两种固体物质,分别加入10g水,使其充分溶解,观察到查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴定管出口部分开始有气泡,滴定后气泡消失 |
| B、锥形瓶用蒸馏水冲洗后随即使用 |
| C、当看到锥形瓶中溶液的颜色发生变化后随即停止了滴定 |
| D、滴定管在用蒸馏水洗净后,即装入标准的酸溶液进行滴定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com