
依据氧化还原反应:2Ag+(aq) + Cu(s) == Cu2+(aq) + 2Ag(s)设计的原电池如图所示。

请回答下列问题:
(1)电极X的材料是 ;电解质溶液Y是 ;
(2)银电极为电池的 极,发生的电极反应为 ;X电极上发生的电极反应为 ;
(3)外电路中的电子是从 电极流向 电极。
科目:高中化学 来源:2016届吉林省高三上学期第二次模拟化学试卷(解析版) 题型:选择题
有A、B、C、D四种短周期元素在周期表中位置如图所示。已知:A2+与C原子的电子数相差2。下列推断不正确的是
…… | C | |||
A | B | …… | D |
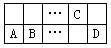
A.A和D组成的化合物是弱电解质且水溶液呈酸性
B.与A同周期且与C同主族的E元素,其最高价氧化物对应水化物在某些化学反应中常作催化剂
C.离子半径:C>A>B
D.B与C形成的化合物是冶金工业的一种原料
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三上学期12月月考理综化学试卷(解析版) 题型:填空题
Ⅰ.(1)工业上合成氨的反应:N2(g)+3H2(g)  2NH3(g) ΔH=-92.60 kJ·mol-1。
2NH3(g) ΔH=-92.60 kJ·mol-1。
①恒温容积固定的密闭容器中发生反应:N2(g)+3H2(g)  2NH3(g),下列说法能说明上述反应达到平衡状态的是____________。
2NH3(g),下列说法能说明上述反应达到平衡状态的是____________。
a.单位时间内生成2n mol NH3的同时生成3n mol H2
b.单位时间内生成6n mol N—H键的同时生成2n mol H—H键
c.用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1∶3∶2
d.混合气体的平均摩尔质量不变
e.容器内的气体密度不变
f.容器内气体的压强不变
(2)已知合成氨反应在某温度下2 L的密闭容器中进行,测得如下数据:
物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
NH3 | 0 | 0.20 | n2 | 1.00 | 1.00 |
根据表中数据计算:
①反应进行到2 h时放出的热量为________ kJ。
②0~1 h内N2的平均反应速率为________ mol·L-1·h-1。
③此温度下该反应的化学平衡常数K=________(保留两位小数)。
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00 mol,化学平衡将向________方向移动(填“正反应”或“逆反应”)。
Ⅱ.(1)二氧化碳是一种重要的温室气体,减少二氧化碳的排放是解决温室效应的有效途径。目前,由二氧化碳合成二甲醚的研究工作已取得了重大进展,其化学反应方程式为2CO2(g)+6H2(g)  CH3OCH3(g)+3H2O(g) ΔH>0。二甲醚气体的燃烧热为1 455 kJ·mol-1,工业上用合成气(CO、H2)直接或间接合成二甲醚。下列有关叙述正确的是________。
CH3OCH3(g)+3H2O(g) ΔH>0。二甲醚气体的燃烧热为1 455 kJ·mol-1,工业上用合成气(CO、H2)直接或间接合成二甲醚。下列有关叙述正确的是________。
A.二甲醚分子中含极性共价键
B.二甲醚作为汽车燃料不会产生污染物
C.二甲醚是非极性分子 D.表示二甲醚燃烧热的热化学方程式为CH3OCH3(g)+3O2(g)===2CO2(g)+3H2O(g) ΔH=-1 455 kJ·mol-1
(2)绿色电源“直接二甲醚燃料电池”的工作原理示意图如图所示:正极为________(填“A电极”或“B电极”),H+移动方向为:由 到 (填A或B),写出A电极的电极反应式:___________。

查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上学期第三次月考化学试卷(解析版) 题型:选择题
常温下某溶液中,由水电离出的c(H+)为1×10—12mol/L,该溶液中一定能大量共存的离子组是
A.K+、Na+、SO42—、NO3— B.Na+、K+、ClO—、CO32—
C.Fe2+、Mg2+、Cl—、SO42— D.NH4+、Cl—、K+、SO32—
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建晨曦、冷曦、正曦、岐滨四校高二上联考化学卷(解析版) 题型:选择题
常温时,纯水中由水电离的c(H+)=a,pH=1的盐酸中由水电离的c(H+)=b,0.2 mol/L的盐酸与0.1 mol/L的氢氧化钠溶液等体积混合后,由水电离的c(H+)=c,则a、b、c的关系正确的是
A.a>b=c B.c>b>a C. a>c>b D.b>c>a
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.反应热就是反应中放出的能量
B.在101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热
C.由C(s,石墨)= C(s,金刚石),ΔH=1.9 kJ·mol-1可知,金刚石比石墨稳定
D.等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多
查看答案和解析>>
科目:高中化学 来源:2016届安徽省皖江名校高三上学期12月联考化学试卷(解析版) 题型:填空题
铁及其化合物有丰富多彩的化学性质。回答下列问题:
(1)铁元素在周期表中的位置为第___________周期第__________族。
(2) FeCl3溶液可用于吸收尾气中的SO2,写出该反应的离子方程式:_____________。
(3)某化学兴趣小组同学用下图装置,充分加热硫酸亚铁晶体(FeSO4.xH2O)至完全分解。
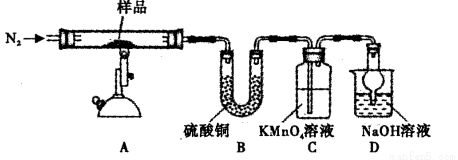
①装置A中需持续通入N2,其目的是
②充分反应一段时间后,小组同学观察到实验现象为:装置A中残留有红棕色固体,装置B中固体变蓝,C中溶液褪色,请写出FeSO4分解的化学方程式:________。
③装置D中干燥管的作用为__________。
④小组同学利用数字化实验仪器测定了不同温度时FeSO4.xH2O分解的质量变化情况,得到下
图关系:
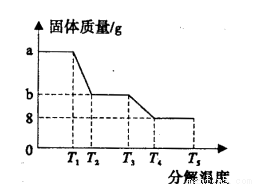
实验结束后后,装置B质量增加12. 6g,结合上图数据,确定FeSO4·xH2O中的x=
查看答案和解析>>
科目:高中化学 来源:2016届湖南省、修水一中高三上学期联考化学试卷(解析版) 题型:选择题
下列事实不能用平衡移动原理来解释的是( )
A.打开啤酒瓶盖,产生大量气泡
B.稀释CH3COOH时,溶液中CH3COO—数目增多
C.工业合成氨常用500℃左右的温度
D.热的纯碱溶液的去污效果比冷的好
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一上学期期中考试化学试卷(解析版) 题型:选择题
氯气的水溶液称“氯水”,氯水中含有多种分子和离子,因此氯水有多重性质,下列有关新制氯水的说法中不正确的是( )
A.新制氯水呈黄绿色,且有刺激性气味,说明氯水中含有Cl2
B.新制氯水滴在蓝色石蕊试纸上,试纸先变红色后褪色,说明氯水中含有Cl2
C.向氯水滴入AgNO3溶液产生白色沉淀,再加稀硝酸沉淀不溶,可说明氯水中含有Cl-
D.新制氯水滴到Na2CO3 溶液中,有气体产生,说明氯水中含有H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com