
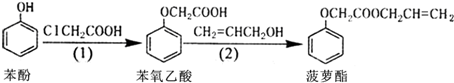
| A. | 苯酚和菠萝酯均可与酸性KMnO4溶液发生反应 | |
| B. | 苯酚、苯氧乙酸和菠萝酯均可与NaOH溶液发生反应 | |
| C. | 步骤(1)中由苯酚生成苯氧乙酸的反应属于取代反应 | |
| D. | 步骤(2)产物中残留的烯丙醇(CH2=CHCH2OH)可用溴水检验 |
分析 苯酚含有酚羟基,可发生颜色反应,苯氧乙酸含有羧基,具有酸性,可发生中和反应,取代反应,菠萝酯含有酯基,可发生水解反应,含有碳碳双键,可发生加成、氧化反应,以此解答该题.
解答 解;A.苯酚含有酚羟基,可与酸性高锰酸钾发生氧化还原反应,菠萝酯含有碳碳双键,可被酸性高锰酸钾氧化,故A正确;
B.苯酚含有酚羟基、苯氧乙酸含有羧基,具有酸性,菠萝酯含有酯基,可发生水解反应,都可与NaOH反应,故B正确;
C.由苯酚生成苯氧乙酸,同时生成HCl,为取代反应,故C正确;
D.菠萝酯和丙烯醇都含有碳碳双键,都能与溴水发生加成反应,不能用溴水鉴别,故D错误.
故选D.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的结构特征和官能团的性质,为解答该题的关键,难度中等.


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②③④ | C. | ①②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯转化为溴苯、苯酚转化为环己醇 | |
| B. | 由乙醇制溴乙烷、由乙烯制溴乙烷 | |
| C. | 乙烯使溴水褪色、乙醇使酸性重铬酸钾溶液变为蓝绿色 | |
| D. | 由乙炔制氯乙烯、由氯乙烯制聚氯乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
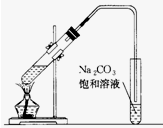 如图是实验室制乙酸乙酯的装置.在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合,然后轻轻地振荡试管,使之混合均匀.
如图是实验室制乙酸乙酯的装置.在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合,然后轻轻地振荡试管,使之混合均匀.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有共价键的晶体一定具有高的熔、沸点及硬度 | |
| B. | 晶格能由大到小:NaI>NaBr>NaCl>NaF | |
| C. | 含阳离子的化合物一定有阴离子 | |
| D. | 空间利用率:面心立方>六方密堆积>体心立方 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.01mol/L | B. | 0.017mol/L | C. | 0.02mol/L | D. | 0.05mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com