
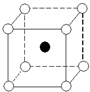
 如图是氯化铯晶体的晶胞结构示意图(晶胞是指晶体中最小的重复单元),其中黑球表示氯离子、白球表示铯离子.已知晶体中2个最近的铯离子的核间距离为a cm,氯化铯的摩尔质量为M g/mol,则氯化铯晶体的密度为( )
如图是氯化铯晶体的晶胞结构示意图(晶胞是指晶体中最小的重复单元),其中黑球表示氯离子、白球表示铯离子.已知晶体中2个最近的铯离子的核间距离为a cm,氯化铯的摩尔质量为M g/mol,则氯化铯晶体的密度为( )| A. | $\frac{2M}{{N}_{A}{a}^{3}}$g/cm3 | B. | $\frac{M}{2{N}_{A}{a}^{3}}$g/cm3 | C. | $\frac{M}{{N}_{A}{a}^{3}}$g/cm3 | D. | $\frac{M{a}^{3}}{{N}_{A}}$g/cm3 |
分析 晶体中2个最近的铯离子的核间距离为a cm,相邻顶点上铯离子核间距离最近,为acm,即晶胞的棱长为acm,体积V=a3cm3,该晶胞中Cs+个数=8×$\frac{1}{8}$=1,Cl-个数为1,根据晶胞密度公式ρ=$\frac{m}{V}$计算密度.
解答 解:晶体中2个最近的铯离子的核间距离为a cm,相邻顶点上铯离子核间距离最近,为acm,即晶胞的棱长为acm,体积V=a3cm3,该晶胞中Cs+个数=8×$\frac{1}{8}$=1,Cl-个数为1,根据晶胞密度公式ρ=$\frac{m}{V}$=$\frac{\frac{M}{{N}_{A}}×1}{{a}^{3}}$=$\frac{M}{{N}_{A}a{\;}^{3}}$g•cm-3,故选C.
点评 本题考查晶胞密度计算,难度不大,应准确计算出晶胞所含微粒数目.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
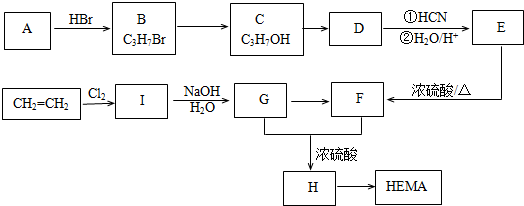
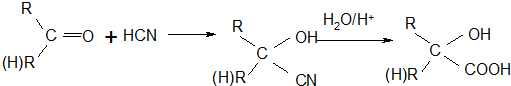
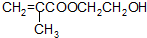 的名称为甲基丙烯酸羟乙酯,
的名称为甲基丙烯酸羟乙酯,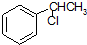 为原料制备
为原料制备 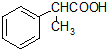 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).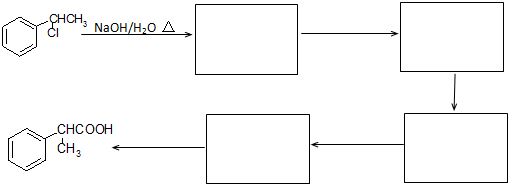
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
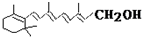 ,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )| A. | 维生素A的分子式为C20H32O | |
| B. | 维生素A不能使溴的四氯化碳溶液褪色 | |
| C. | 该有机物能发生取代反应 | |
| D. | 1mol维生素A 在催化剂作用下最多可与7molH2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
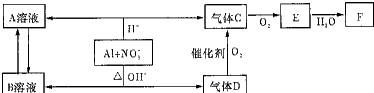
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯可用作水果的催熟剂 | |
| B. | 黄铜(铜锌合金)制作的铜锣不易产生铜绿 | |
| C. | 二氧化硫可用作食品的漂白剂 | |
| D. | 交警可用酸性重铬酸钾来检测司机是否酒驾 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com