
摩尔盐[xFeSO4·y(NH4)2SO4·zH2O]是一种重要化工原料。其组成可通过下列实验测定:
① 称取1.5680 g样品,准确配成100 mL溶液A。
② 量取25.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固体0.4660 g。
③ 再量取25.00 mL溶液A,滴加适量稀硫酸,用0.0200 mol·L-1KMnO4溶液滴定至终点,生成Mn2+,消耗KMnO4溶液10.00 mL。
(1)已知室温下BaSO4的Ksp=1.1×10-10,欲使溶液中c(SO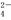 )≤1.0×10-5 mol·L-1,应保持溶液中c(Ba2+)≥ mol·L-1。
)≤1.0×10-5 mol·L-1,应保持溶液中c(Ba2+)≥ mol·L-1。
(2)③中发生反应的离子方程式为 ,滴定终点的现象是 。
(3)通过计算确定样品的组成(必须写出计算过程)。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2017届宁夏高三上月考四化学试卷(解析版) 题型:填空题
【化学——选修物质结构与性质】
X是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y基态原子的3p轨道上有2个未成对电子。元素Z 的原子最外层电子数是其内层的3倍。回答下列问题:
(1)元素X在元素周期表中位于 区,单质X的晶体类型为 ,其中X原子的配位数为 。
(2)已知元素Y可与元素Z的相对原子质量只差为16,则元素Y基态原子的外围电子排布图为 ,其同周期元素中,第一电离能最大的是________________(写元素符号)。元素Y的含氧酸中,酸性最强的是_____________(写化学式),该酸根离子的立体构型为_____________。
(3)Z的氢化物在乙醇中的溶解度大于Y的氢化物,其原因是 。
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为 。
(5)X与Y形成的一种化合物的立方晶胞如图所示。
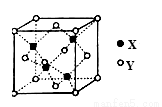
该化合物的化学式为_______________,已知此晶体的密度为ρg·cm–3,阿伏伽德罗常数为NA,则此晶胞中X与Y的最近距离是 cm。(写出计算式,不要求计算结果。)
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:选择题
下列离子在指定溶液中一定能大量共存的是
A.加入Al能放出H2的溶液中:Fe2+、K+、NO 、Cl-
、Cl-
B.在pH=13的溶液中:Na+、AlO2-、NO 、S2-、SO
、S2-、SO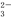
C.由水电离的c(H+)=10-12mol·L-1的溶液中:Cl-、NO 、NH
、NH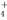 、F-
、F-
D.NaHCO3溶液中:K+、Na+、SO 、Al3+
、Al3+
查看答案和解析>>
科目:高中化学 来源:2017届江西师大附中高三上学期期中化学试卷(解析版) 题型:选择题
红色溶液X中通入气体Y,溶液逐渐褪色,下列对X、Y的推断正确的是( )
A.若X为品红溶液,则Y一定是Cl2或SO2
B.若X为含酚酞的氢氧化钠溶液,则Y可能是SO2
C.若X为含KSCN的氯化铁溶液,则Y一定是HI
D.若X为含硫酸氢钠的石蕊溶液,则Y可能是SO2
查看答案和解析>>
科目:高中化学 来源:2017届江西师大附中高三上学期期中化学试卷(解析版) 题型:选择题
下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | 1?己醇的沸点比己烷的沸点高 | 1?己醇和己烷可通过蒸馏初步分离 |
B | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
C | 乙二酸可与KMnO4溶液发生反应 | 乙二酸具有酸性 |
D | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上学期期中化学卷(解析版) 题型:选择题
下列描述正确的是( )
A. 向甲苯中滴入适量浓溴水,振荡后静置,溶液上层呈橙红色,下层几乎无色,说明甲苯和溴发生了取代反应
B. 将硫的酒精溶液滴入一定量的热水中得微蓝色透明液体,用激光笔照射,有丁达尔效应,说明微蓝色液体为胶体
C. 某钠盐溶液中加入盐酸酸化的硝酸钡溶液有白色沉淀,说明该钠盐是硫酸钠或硫酸氢钠
D. 锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上学期期中化学卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.1 mol CH3+含电子数为10NA
B.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA
C.标准状况下,22.4 L水中含有原子总数为3NA
D.1molCl2完全溶于水后,转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省娄底市等五校高二上期中化学卷(解析版) 题型:选择题
下列对“改变反应条件,导致化学反应速率改变”的原因描述不正确的是
A.增大反应物的浓度,活化分子百分数增加,反应速率加快
B.增大气体反应体系的压强,单位体积中活化分子数增多,气体反应速率加快
C.升高反应的温度,活化分子百分数增加,有效碰撞的几率提高,反应速率增大
D.催化剂通过改变反应路径,使反应所需的活化能降低,反应速率增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林两省八校高一上学期期中化学试卷(解析版) 题型:实验题
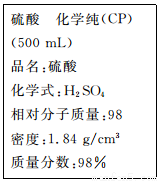
(1)该硫酸的物质的量浓度为____________mol/L。
(2)某化学小组进行硫酸酸性实验探究时,需要240 ml,4.6 mol.L-l的稀硫酸,则在配制时需要取上述浓硫酸_____________mL。
(3)叙述将上述浓硫酸进行稀释的实验操作:____________________。
(4)在配制4.6 mol.L-l稀硫酸的过程中,下列情况对所配制的硫酸溶液的物质的量浓度有何影响?
①用量筒量取浓硫酸时俯视量筒刻度线_____________(填“偏高”、“偏低”或“无影响”,下同);
②未经冷却趁热将溶液注入容量瓶中:_____________;
③仰视容量瓶刻度线定容:__________________;
④移液时不慎将少量溶液滴在容量瓶外面:_____________;
(5)实验过程中出现下列情况应如何处理?
①向容量瓶中加入蒸馏水,液面离容量瓶颈刻度线下1~2 cm时,应_____________。
②加蒸馏水时不慎超过了容量瓶颈刻度线,应_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com