
�跴Ӧ��Fe(s)+CO2(g) ![]() FeO(s)+CO(g)��ƽ�ⳣ��ΪK1��
FeO(s)+CO(g)��ƽ�ⳣ��ΪK1��
��Ӧ��Fe(s)+H2O(g) ![]() FeO(s)+H2(g)��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶��£� K1��K2��ֵ���£�
FeO(s)+H2(g)��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶��£� K1��K2��ֵ���£�
| T(K) | K1 | K2 |
| 973 | 1.47 | 2.36 |
| 1173 | 2.15 | 1.67 |
��1��ƽ�ⳣ��K1�ı���ʽΪ ________________ ��
��2�����з�Ӧ�� CO2(g) +H2(g) ![]() CO(g) +H2O(g);��H>0������һ�� ��������š��� �ȷ�Ӧ��Ҫʹ��Ӧ����һ�������½�����ƽ�������ƶ����ɲ�ȡ�Ĵ�ʩ���� ��
CO(g) +H2O(g);��H>0������һ�� ��������š��� �ȷ�Ӧ��Ҫʹ��Ӧ����һ�������½�����ƽ�������ƶ����ɲ�ȡ�Ĵ�ʩ���� ��
A.��С��Ӧ�����ݻ� B.����Ӧ�����ݻ� C.�����¶�
D.�����¶� E.ʹ�ú��ʵĴ��� F.�跨����CO����
��3������ӦFe(s)+CO2(g) ![]() FeO(s)+CO(g)���¶�T1�½��У�Fe(s)+H2O(g)
FeO(s)+CO(g)���¶�T1�½��У�Fe(s)+H2O(g) ![]() FeO(s)+H2(g)���¶�T2�½��У���֪T1>T2����c(CO2)>c(CO)��������������ͬ���������ߵķ�Ӧ���� ������ţ���
FeO(s)+H2(g)���¶�T2�½��У���֪T1>T2����c(CO2)>c(CO)��������������ͬ���������ߵķ�Ӧ���� ������ţ���
A.ǰ�ߴ� B.���ߴ� C.һ���� D.���ж�
��4������ͼ��ͼ��vΪ���ʣ���Ϊ������İٷֺ�����TΪ�¶ȣ�
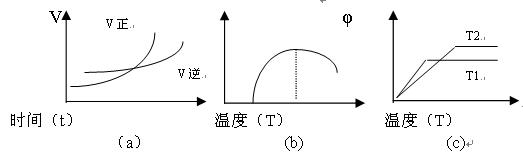
���з��Ϸ�Ӧ�ٵ��� _________ ����ͼ����ţ���ͬ�������Ϸ�Ӧ�ڵ��� ___ ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���跴Ӧ��Fe(s)+CO2(g)![]() FeO(s)+CO(g) ��H = Q1��ƽ�ⳣ��ΪK1��
FeO(s)+CO(g) ��H = Q1��ƽ�ⳣ��ΪK1��
��Ӧ��Fe(s)+H2O(g)![]() FeO(s)+H2(g) ��H = Q2��ƽ�ⳣ��ΪK 2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�
FeO(s)+H2(g) ��H = Q2��ƽ�ⳣ��ΪK 2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�
| �¶�( T ) | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
(1)���ϱ����ƶϣ���Ӧ����_______(��š�������)�ȷ�Ӧ��K2����ѧ����ʽΪ ��
(2)���з�Ӧ��H2(g)+CO2(g)![]() CO(g)+H2O(g)��H = Q3 �ٸ��ݷ�Ӧ������Ƶ���K1��K2��K3�Ĺ�ϵʽK3=_____________�����ƶϷ�Ӧ����________(��š�������)�ȷ�Ӧ��Ҫʹ��Ӧ����һ�������½�����ƽ�����ƣ��ɲ�ȡ�Ĵ�ʩ��__________��
CO(g)+H2O(g)��H = Q3 �ٸ��ݷ�Ӧ������Ƶ���K1��K2��K3�Ĺ�ϵʽK3=_____________�����ƶϷ�Ӧ����________(��š�������)�ȷ�Ӧ��Ҫʹ��Ӧ����һ�������½�����ƽ�����ƣ��ɲ�ȡ�Ĵ�ʩ��__________��
A����С������� B�������¶� C��ʹ�ú��ʵĴ���
D���跨����CO���� E�������¶�
�ڸ��ݷ�Ӧ������Ƶ���Q1��Q2��Q3�Ĺ�ϵʽQ3 =_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010�꽭��ʡ������ѧ��һ�ڶ�ѧ�����п��Ի�ѧ��ʵ��ࣩ���� ���ͣ������
��10�֣��跴Ӧ��Fe(s)+CO2(g)  FeO(s)+CO(g)��ƽ�ⳣ��ΪK1��
FeO(s)+CO(g)��ƽ�ⳣ��ΪK1��
��Ӧ��Fe(s)+H2O(g)  FeO(s)+H2(g)��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶��£� K1��K2��ֵ���£�
FeO(s)+H2(g)��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶��£� K1��K2��ֵ���£�
| T(K) | K1 | K2 |
| 973 | 1.47 | 2.36 |
| 1173 | 2.15 | 1.67 |
 CO(g) +H2O(g);��H>0������һ�� ��������š��� �ȷ�Ӧ��Ҫʹ��Ӧ����һ�������½�����ƽ�������ƶ����ɲ�ȡ�Ĵ�ʩ���� ��
CO(g) +H2O(g);��H>0������һ�� ��������š��� �ȷ�Ӧ��Ҫʹ��Ӧ����һ�������½�����ƽ�������ƶ����ɲ�ȡ�Ĵ�ʩ���� �� FeO(s)+CO(g)���¶�T1�½��У�Fe(s)+H2O(g)
FeO(s)+CO(g)���¶�T1�½��У�Fe(s)+H2O(g)  FeO(s)+H2(g)���¶�T2�½��У���֪T1>T2����c(CO2)>c(CO)��������������ͬ���������ߵķ�Ӧ���� ������ţ���
FeO(s)+H2(g)���¶�T2�½��У���֪T1>T2����c(CO2)>c(CO)��������������ͬ���������ߵķ�Ӧ���� ������ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012��ɽ��ʡƽң��ѧ�߶���ѧ�����п��Ի�ѧ�������Ծ� ���ͣ������
��10�֣��跴Ӧ��Fe(s)+CO2(g) FeO(s)+CO(g) ��H = Q1��ƽ�ⳣ��ΪK1����Ӧ��Fe(s)+H2O(g)
FeO(s)+CO(g) ��H = Q1��ƽ�ⳣ��ΪK1����Ӧ��Fe(s)+H2O(g) FeO(s)+H2(g) ��H = Q2��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�
FeO(s)+H2(g) ��H = Q2��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�
| �¶�( T ) | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
 CO(g)+H2O(g)��H = Q
CO(g)+H2O(g)��H = Q ��Ҫʹ��Ӧ����һ�������½�����ƽ�����ƣ��ɲ�ȡ�Ĵ�ʩ��__________��
��Ҫʹ��Ӧ����һ�������½�����ƽ�����ƣ��ɲ�ȡ�Ĵ�ʩ��__________�� ��CO���� E�������¶�
��CO���� E�������¶��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�������ʡ������ѧ�����п��Ի�ѧ�Ծ� ���ͣ������
���跴Ӧ��Fe(s)+CO2(g) FeO(s)+CO(g) ��H = Q1��ƽ�ⳣ��ΪK1��
FeO(s)+CO(g) ��H = Q1��ƽ�ⳣ��ΪK1��
��Ӧ��Fe(s)+H2O(g) FeO(s)+H2(g)
��H = Q2��ƽ�ⳣ��ΪK 2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�
FeO(s)+H2(g)
��H = Q2��ƽ�ⳣ��ΪK 2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�
|
�¶�( T ) |
K1 |
K2 |
|
973 |
1.47 |
2.38 |
|
1173 |
2.15 |
1.67 |
(1)���ϱ����ƶϣ���Ӧ����_______(��š�������)�ȷ�Ӧ��K2����ѧ����ʽΪ ��
(2)���з�Ӧ��H2(g)+CO2(g) CO(g)+H2O(g)
��H = Q3 �ٸ��ݷ�Ӧ������Ƶ���K1��K2��K3�Ĺ�ϵʽK3=_____________�����ƶϷ�Ӧ����________(��š�������)�ȷ�Ӧ��Ҫʹ��Ӧ����һ�������½�����ƽ�����ƣ��ɲ�ȡ�Ĵ�ʩ��__________��
CO(g)+H2O(g)
��H = Q3 �ٸ��ݷ�Ӧ������Ƶ���K1��K2��K3�Ĺ�ϵʽK3=_____________�����ƶϷ�Ӧ����________(��š�������)�ȷ�Ӧ��Ҫʹ��Ӧ����һ�������½�����ƽ�����ƣ��ɲ�ȡ�Ĵ�ʩ��__________��
A����С������� B�������¶� C��ʹ�ú��ʵĴ���
D���跨����CO���� E�������¶�
�ڸ��ݷ�Ӧ������Ƶ���Q1��Q2��Q3�Ĺ�ϵʽQ3 =_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010�꽭��ʡ��������У�����߶���ѧ�����п��Ի�ѧ�Ծ� ���ͣ������
�跴Ӧ��Fe(S)+CO2(g)  FeO(S)+CO(g)��ƽ�ⳣ��Ϊ
FeO(S)+CO(g)��ƽ�ⳣ��Ϊ ����Ӧ��Fe(S)+H2O(g)
����Ӧ��Fe(S)+H2O(g)  FeO(S)+H2(g)��ƽ�ⳣ��Ϊ
FeO(S)+H2(g)��ƽ�ⳣ��Ϊ ���ڲ�ͬ�¶��£�
���ڲ�ͬ�¶��£� ��
�� ��ֵ���£�
��ֵ���£�
|
�¶� |
|
|
|
|
1.47 |
2.38 |
|
1173 |
2.15 |
1.67 |
(1)���ϱ������ƶϣ���Ӧ����_______________ (����������š�)�ȷ�Ӧ��
(2)���з�Ӧ��H2(g)+CO2(g)
 H2O(g)+CO(g)д���÷�Ӧ��ƽ�ⳣ��K3����ѧ����ʽ��K
H2O(g)+CO(g)д���÷�Ӧ��ƽ�ⳣ��K3����ѧ����ʽ��K =____________��
=____________��
(3)���ݷ�Ӧ����ڣ����Ƶ���K ��K
��K ��K
��K ֮��Ĺ�ϵʽ_______________���ݴ˹�ϵʽ���ϱ����ݣ�Ҳ���ƶϳ���Ӧ���ǡ����ȡ����ǡ����ȡ���Ӧ���ʣ�Ҫʹ��Ӧ����һ�������½�����ƽ��������Ӧ�����ƶ����ɲ�ȡ�Ĵ�ʩ��_____________(��д���)��
֮��Ĺ�ϵʽ_______________���ݴ˹�ϵʽ���ϱ����ݣ�Ҳ���ƶϳ���Ӧ���ǡ����ȡ����ǡ����ȡ���Ӧ���ʣ�Ҫʹ��Ӧ����һ�������½�����ƽ��������Ӧ�����ƶ����ɲ�ȡ�Ĵ�ʩ��_____________(��д���)��
A����С��Ӧ�����ݻ� B������Ӧ�����ݻ� C�������¶�
D�������¶� E��ʹ�ú��ʵĴ��� F���跨����CO����
(4)ͼl��2��ʾ�÷�Ӧ����ʱ��t �ﵽƽ�⡢��ʱ��t
�ﵽƽ�⡢��ʱ��t �ֱ���ı�ij�������������仯�������
�ֱ���ı�ij�������������仯�������

��ͼl��ʱ��t �����ı��������_____________________________
�����ı��������_____________________________
��ͼ2��ʱ��t �����ı��������________________
�����ı��������________________
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com