
 ZrC��SiO2��2CO�����÷�Ӧ���������뻹ԭ����������Ϊ ��
ZrC��SiO2��2CO�����÷�Ӧ���������뻹ԭ����������Ϊ �� ��Na2ZrO3+��CO2+��H2O
��Na2ZrO3+��CO2+��H2O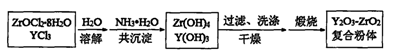
 Na2ZrO3+CO2+H2O��3�֣�
Na2ZrO3+CO2+H2O��3�֣� Na2ZrO3+CO2+H2O���������������������ȵ���ҪĿ�������������ˮ����ֹZrO2+��ˮ�⣻��2���ٶ�ͼ��֪���������������ֽⷴӦ����ӦʽΪZrOCl2+2NH3?H2O+H2O=Zr(OH)4��+2NH4Cl���ڵ�Y3+������ȫʱ����Y(OH)3(s)
Na2ZrO3+CO2+H2O���������������������ȵ���ҪĿ�������������ˮ����ֹZrO2+��ˮ�⣻��2���ٶ�ͼ��֪���������������ֽⷴӦ����ӦʽΪZrOCl2+2NH3?H2O+H2O=Zr(OH)4��+2NH4Cl���ڵ�Y3+������ȫʱ����Y(OH)3(s) Y3+(aq)+3OH��(aq)��֪��c(OH��)=
Y3+(aq)+3OH��(aq)��֪��c(OH��)= =
=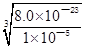 =2.0��10��6mol?L��1����Zr(OH)4(s)
=2.0��10��6mol?L��1����Zr(OH)4(s) Zr4+(aq)+4OH��(aq)��֪��c(Zr4+)=
Zr4+(aq)+4OH��(aq)��֪��c(Zr4+)=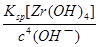 =
= mol?L��1=4.0��10��26mol?L��1����1nm<30nm<100nm����÷�ɢϵ���ڽ��塣
mol?L��1=4.0��10��26mol?L��1����1nm<30nm<100nm����÷�ɢϵ���ڽ��塣

 ���ݼ���ϵ�д�
���ݼ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 Cu+H2O����Ӧ����ͼ�е����� ������ţ������з�Ӧ����������7���� ��
Cu+H2O����Ӧ����ͼ�е����� ������ţ������з�Ӧ����������7���� ��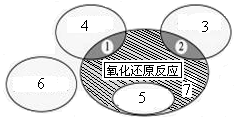
A��2H2+O2 2H2O 2H2O |
B��2NaHCO3 Na2CO3+H2O+CO2�� Na2CO3+H2O+CO2�� |
| C��Zn+H2SO4=ZnSO4+H2�� |
D��CuO+CO Cu+CO2 Cu+CO2 |
 N2+6NH4Cl
N2+6NH4Cl�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| A��Na2CO3 | B��KMnO4 | C��XeO3 | D��Na2SO3 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������n[Cu(NO3)2]��n[CuSO4]��1��1 |
| B���μӷ�Ӧ��n(Cu2S)��n(HNO3)��1��5 |
| C����Ӧ��Cu2S������������������ԭ�� |
| D��1 mol Cu2S�μӷ�Ӧʱ��8 mol����ת�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
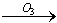 BrO��
BrO��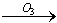 BrO2-
BrO2-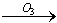 BrO3-�������й�˵����ȷ����
BrO3-�������й�˵����ȷ����| A��������������������ˮԭ����ͬ���������ý�������ԭ�� |
| B�������������������ɱ������������� |
| C��BrO- 3�����Ա�O3ǿ |
| D�����������εĹ����Ǹ�ˮ�����ĸ���Ӧ���������������BrO3-�IJ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
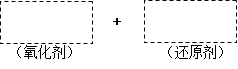
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com