
���������п���AgNO3��Һ�ζ�Cl����Һ������K2CrO4Ϊָʾ�����ﵽ�ζ��յ�ʱ��Һ���Ϊ50mL��c��Cl���� = 10��5 mol��L��1��AgNO3��CrO42�� ����ש��ɫ��Ag2CrO4��������֪Ksp(AgCl) = 1.77��10��10�� Ksp(AgI) = 8.51��10��17��Ksp(Ag2CrO4) = 1.12��10��12����������ʵ��������й����ݣ�����˵����ȷ����
A�������£���AgCl�����AgCl��Һ�м���NaCl���壬AgCl������������
B���ζ��յ�ʱ����Һ��CrO42����Ũ��ԼΪ3.6��10��3 mol��L��1
C����10mL0.1moL/L AgNO3��Һ�еμ�3��5��0.1moL/L NaCl��Һ����AgCl�������ٵμ�KI��Һ������AgI�������ܹ�˵��Ksp(AgI)�� Ksp(AgCl)
D������0.1 mol��L��1��KI��Һ����K2CrO4��ָʾ��
B
��������A����ȷ������������Ũ�Ȼ������Ȼ������塣�����յ�����Һ��c��Cl���� = 10��5 mol��L��1������������Ũ����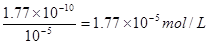 �������Һ��CrO42����Ũ��
�������Һ��CrO42����Ũ�� 3.6��10��3 mol��L��1��B��ȷ��C����ȷ����Ϊ�������ǹ����ģ�����⻯�غ���������Ӧ���ɵ⻯��������D����ȷ����Ϊ�⻯�����ܶȻ�����С���Ȼ����ģ��������ɵij����ǵ⻯�����������Ȼ�������ѡB��
3.6��10��3 mol��L��1��B��ȷ��C����ȷ����Ϊ�������ǹ����ģ�����⻯�غ���������Ӧ���ɵ⻯��������D����ȷ����Ϊ�⻯�����ܶȻ�����С���Ȼ����ģ��������ɵij����ǵ⻯�����������Ȼ�������ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���йظû����������˵������ȷ���ǣ�������
���йظû����������˵������ȷ���ǣ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㽭ʡ����һ��2011��2012ѧ��߶���ѧ����ĩ���Ի�ѧ���� ���ͣ�013
|
���������п���AgNO3��Һ�ζ�Cl����Һ������K2CrO4Ϊָʾ�����ﵽ�ζ��յ�ʱ��Һ���Ϊ50 mL��c(Cl��)��10��5 mol��L��1��AgNO3��CrO42������ש��ɫ��Ag2CrO4��������֪Ksp(AgCl)��1.77��10��10��Ksp(AgI)��8.51��10��17��Ksp(Ag2CrO4)��1.12��10��12����������ʵ��������й����ݣ�����˵����ȷ���� | |
| [����] | |
A�� |
�����£���AgCl�����AgCl��Һ�м���NaCl���壬AgCl������������ |
B�� |
�ζ��յ�ʱ����Һ��CrO42����Ũ��ԼΪ3.6��10��3 mol��L��1 |
C�� |
��0.1 moL/L��AgNO3��Һ�еμ�3��5��0.1 moL/L��NaCl��Һ����AgCl�������ٵμ�KI��Һ������AgI�������ܹ�˵��Ksp(AgI)��Ksp(AgCl) |
D�� |
����0.1 mol��L��1��KI��Һ����K2CrO4��ָʾ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012���㽭ʡ����һ�и���5��ģ�⿼�������ۺϻ�ѧ�Ծ����������� ���ͣ���ѡ��
���������п���AgNO3��Һ�ζ�Cl����Һ������K2CrO4Ϊָʾ�����ﵽ�ζ��յ�ʱ��Һ���Ϊ50mL��c��Cl���� = 10��5 mol��L��1��AgNO3��CrO42�� ����ש��ɫ��Ag2CrO4��������֪Ksp(AgCl) = 1.77��10��10��Ksp(AgI) = 8.51��10��17��Ksp(Ag2CrO4) = 1.12��10��12����������ʵ��������й����ݣ�����˵����ȷ����
| A�������£���AgCl�����AgCl��Һ�м���NaCl���壬AgCl������������ |
| B���ζ��յ�ʱ����Һ��CrO42����Ũ��ԼΪ3.6��10��3 mol��L��1 |
| C����10mL0.1moL/L AgNO3��Һ�еμ�3��5��0.1moL/L NaCl��Һ����AgCl�������ٵμ�KI��Һ������AgI�������ܹ�˵��Ksp(AgI)�� Ksp(AgCl) |
| D������0.1 mol��L��1��KI��Һ����K2CrO4��ָʾ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com