
| A. | 离子结构示意图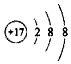 ,可以表示35Cl-,也可以表示37Cl- ,可以表示35Cl-,也可以表示37Cl- | |
| B. | 电子式 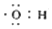 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 | |
| C. | 比例模型 可以表示甲烷分子,也可以表示四氯化碳分子 可以表示甲烷分子,也可以表示四氯化碳分子 | |
| D. | 聚丙烯的结构简式为: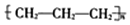 |
分析 A.35Cl-和37Cl-都是氯离子,其离子结构示意图相同;
B.羟基为中性原子团,氢氧根离子带有电荷,二者离子结构示意图不同;
C.甲烷分子中碳原子的相对体积较大,而四氯化碳中氯原子的原子半径带有碳原子;
D.聚丙烯的链节主链含有2个C.
解答 解:A.35Cl-和37Cl-的离子结构示意图相同,都可以用 表示,故A正确;
表示,故A正确;
B.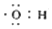 为中性原子团,只能表示羟基,不能表示氢氧根离子,故B错误;
为中性原子团,只能表示羟基,不能表示氢氧根离子,故B错误;
C. 的中心原子的相对体积较大,可以表示甲烷分子,由于氯原子的原子半径大于碳原子,则该比例模型不能表示四氯化碳,故C错误;
的中心原子的相对体积较大,可以表示甲烷分子,由于氯原子的原子半径大于碳原子,则该比例模型不能表示四氯化碳,故C错误;
D.聚丙烯为高分子化合物,聚丙烯是由丙烯不饱和的碳原子相互加成得到的,其结构简式为 ,故D错误;
,故D错误;
故选A.
点评 本题考查常见化学用语的表示方法,题目难度中等,涉及比例模型、电子式、结构简式、离子结构示意图等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.


科目:高中化学 来源: 题型:选择题
| A. | 常温下,48gO3含有的氧原子数3NA | |
| B. | 33.6LCO中含有的原子数是3NA | |
| C. | 0.5mol•L-1CaCl2溶液中含Cl-数目为NA | |
| D. | 17gNH3所含的电子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 发展清洁能源 | B. | 增加植被面积 | C. | 燃烧煤炭供热 | D. | 选择绿色出行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 具有相同质子数的微粒一定属于同一种元素 | |
| B. | H2O和H2O2互为同素异形体 | |
| C. | 含有金属元素的离子不一定是阳离子 | |
| D. | 同种元素的原子中,中子数和质子数一定都相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径:W>X | |
| B. | 含氧酸的酸性:W>Z | |
| C. | 气态氢化物的稳定性:W<Y | |
| D. | 若W与X原子序数差为5,则形成化合物的化学式为X3W2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤的反应类型相同 | B. | ⑥⑦的反应类型不同 | ||
| C. | ④与其他8个反应的类型都不同 | D. | ①③⑧属于同一种反应类型 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
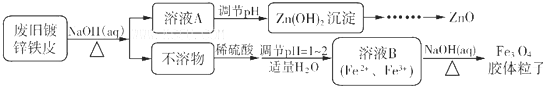
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,AgCl 在饱和 NaCl 溶液中的 KSP 比在纯水中的 KSP 小 | |
| B. | 向 AgCl 的悬浊液中加入 KI 溶液,沉淀由白色转化为黄色 | |
| C. | 向 AgCl 的饱和溶液中加入 NaCl 晶体,有 AgCl 析出且溶液中 c(Ag+)=c(Cl-) | |
| D. | 将 0.001 mol•L-1 的 AgNO3 溶液滴入 KCl 和 KI 的混合溶液中,一定先产生 AgI 沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com