
| A.配平后水的化学计量数为4 |
| B.反应后溶液呈酸性 |
| C.配平后氧化剂与还原剂的物质的量之比为3∶28 |
| D.氧化产物为AsO43—和SO42— |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在硬质试管中隔绝空气高温加热固体混合物时,有0.6 g碳参加了反应 |
| B.试管中发生的所有氧化还原反应共转移电子0.15 mol |
| C.反应后试管中剩余的固体混合物的总质量为7.2 g |
| D.反应生成铜和氧化亚铜的总物质的量为0.1 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.实验室用NH4Cl 和Ca(OH)2制备NH3 |
| B.工业上电解熔融状态Al2O3制备Al |
| C.工业上利用合成氨实现人工固氮 |
| D.Na2O2用作呼吸面具的供氧剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

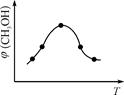
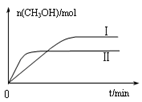
 CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X的化学式为AgS |
| B.银针验毒时,空气中氧气失去电子 |
| C.反应中Ag和H2S均是还原剂 |
| D.每生成1mo1X,反应转移2mo1电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 → Mn2++NO3-+H2O。下列叙述中正确的是( )
→ Mn2++NO3-+H2O。下列叙述中正确的是( )| A.该反应中NO2-是还原剂 |
| B.反应过程中溶液的pH 减小 |
| C.生成1 mol NaNO3时消耗2.5 mol KMnO4 |
D. 中的粒子是OH- 中的粒子是OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该反应显示硫酸具有酸性 | B.NH4CuSO3中硫元素被氧化 |
| C.刺激性气味的气体是氨气 | D.反应中硫酸作氧化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com