
Ģ¼µ„ÖŹŌŚ¹¤ŅµÉĻÓŠ¶ąÖÖÓĆĶ¾”£ĄżČē½¹ĢææÉÓĆĄ“ÖĘČ”Ė®ĆŗĘų”¢Ņ±Į¶½šŹō£¬»īŠŌĢææÉ“¦Ąķ“óĘųĪŪČ¾ĪļNO”£
Ņ»¶ØĢõ¼žĻĀ£¬ŌŚ2 LĆܱÕČŻĘ÷ÖŠ¼ÓČėNOŗĶ»īŠŌĢæ£ØĪŽŌÓÖŹ£©·“Ӧɜ³ÉĘųĢåAŗĶB”£µ±ĪĀ¶ČŌŚT1”ꏱ£¬²āµĆø÷ĪļÖŹĘ½ŗāŹ±ĪļÖŹµÄĮæČēĻĀ±ķ£ŗ
| | »īŠŌĢæ (mol) | NO (mol) | A (mol) | B (mol) |
| ³õŹ¼ | 2.030 | 0.100 | 0 | 0 |
| Ę½ŗā | 2.000 | 0.040 | 0.030 | 0.030 |
£Ø1£©0.015mol/(L”¤min)£¬Š”ÓŚ£Ø3·Ö£©
£Ø2£©a b£Ø2·Ö£©
£Ø3£© £Ø1·Ö£© ²»ÄÜ£¬ĪŽ·ØČ·¶ØT1”¢T2µÄĻą¶ŌøßµĶ”££Ø»ņÄÜ£¬µ±T1>T2Ź±£¬·“Ó¦ŹĒĪüČČ·“Ó¦£¬µ±T1<T2Ź±£¬·“Ó¦ŹĒ·ÅČČ·“Ó¦£Ø2·Ö£©
£Ø1·Ö£© ²»ÄÜ£¬ĪŽ·ØČ·¶ØT1”¢T2µÄĻą¶ŌøßµĶ”££Ø»ņÄÜ£¬µ±T1>T2Ź±£¬·“Ó¦ŹĒĪüČČ·“Ó¦£¬µ±T1<T2Ź±£¬·“Ó¦ŹĒ·ÅČČ·“Ó¦£Ø2·Ö£©
½āĪöŹŌĢā·ÖĪö£ŗ
£Ø1£©øĆ·“Ó¦ĪŖ£ŗ C + 2NO = CO2 + N2
ĘšŹ¼Įæ 2.030 0.100 0 0
Ę½ŗāĮæ 2.000 0.040 0.030 0.030
NOĖŁĀŹĪŖ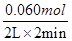 =0.015mol/(L”¤min)£¬·“Ó¦µÄĖŁĀŹĖę×ÅÅØ¶ČµÄ¼õŠ”¶ų¼õŠ”£¬¹ŹæŖŹ¼æģ£¬Ź±¼äŠ”ÓŚ1min£»
=0.015mol/(L”¤min)£¬·“Ó¦µÄĖŁĀŹĖę×ÅÅØ¶ČµÄ¼õŠ”¶ų¼õŠ”£¬¹ŹæŖŹ¼æģ£¬Ź±¼äŠ”ÓŚ1min£»
£Ø2£©a”¢CĪŖ¹ĢĢ壬øıäĘäĮ棬²»Ź¹»ÆŃ§Ę½ŗāŅĘ¶Æ£¬b”¢Ōö“óŃ¹ĒæĘ½ŗā³ÆĢå»ż¼õŠ”µÄ·½ĻņŅĘ¶Æ£¬¼“ÕżĻņ£¬×Ŗ»ÆĀŹŌö“ó£»c”¢øıäĪĀ¶Č£¬Ę½ŗāŅĘ¶Æ£¬×Ŗ»ÆĀŹøı䣻d”¢¼õŠ”Éś³ÉĪļÅØ¶Č£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬æÉŅŌøıä×Ŗ»ÆĀŹ”£
£Ø3£©øł¾ŻK±ä»Æ£¬·ÖĪöĘ½ŗāŅĘ¶Æ·½Ļņ£¬øł¾ŻĪĀ¶ČµÄ±ä»ÆæÉŅŌĘĄÅŠµÄĪüČČ»¹ŹĒ·ÅČČ”£
æ¼µć£ŗ»Æѧ·“Ó¦ĖŁĀŹ¼°»ÆŃ§Ę½ŗāŅĘ¶Æ”¢»ÆŃ§Ę½ŗā³£Źż”¢»Æѧ·“Ó¦ĖŁĀŹĻą¹Ų¼ĘĖć”£


 ČŹ°®Ó¢ÓļĶ¬²½Į·Ļ°²įĻµĮŠ“š°ø
ČŹ°®Ó¢ÓļĶ¬²½Į·Ļ°²įĻµĮŠ“š°ø ѧĻ°Źµ¼łŌ°µŲĻµĮŠ“š°ø
ѧĻ°Źµ¼łŌ°µŲĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
·“Ó¦aA£Øg£©+bB£Øg£© cC£Øg£©£Ø”÷H£¼0£©ŌŚµČČŻĢõ¼žĻĀ½ųŠŠ”£øıäĘäĖū·“Ó¦Ģõ¼ž£¬ŌŚ¢ń”¢¢ņ”¢¢ó½×¶ĪĢåĻµÖŠø÷ĪļÖŹÅضČĖꏱ¼ä±ä»ÆµÄĒśĻßČēĻĀĶ¼ĖłŹ¾£ŗ
cC£Øg£©£Ø”÷H£¼0£©ŌŚµČČŻĢõ¼žĻĀ½ųŠŠ”£øıäĘäĖū·“Ó¦Ģõ¼ž£¬ŌŚ¢ń”¢¢ņ”¢¢ó½×¶ĪĢåĻµÖŠø÷ĪļÖŹÅضČĖꏱ¼ä±ä»ÆµÄĒśĻßČēĻĀĶ¼ĖłŹ¾£ŗ 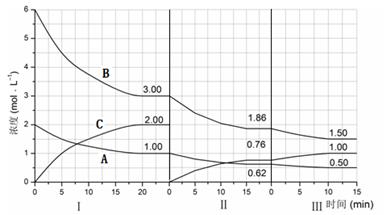
»Ų“šĪŹĢā£ŗ
£Ø1£©·“Ó¦µÄ»Æѧ·½³ĢŹ½ÖŠ£¬a£ŗb£ŗcĪŖ £»
£Ø2£©BµÄĘ½ŗā×Ŗ»ÆĀŹ¦Į¢ń£ØB£©”¢¦Į¢ņ£ØB£©”¢¦Į¢ó£ØB£©ÖŠ×ī“óµÄŹĒ £¬ĘäÖµŹĒ £»
£Ø3£©ÓɵŚŅ»“ĪĘ½ŗāµ½µŚ¶ž“ĪĘ½ŗā£¬Ę½ŗāŅĘ¶ÆµÄ·½ĻņŹĒ £¬²ÉČ”µÄ“ėŹ©ŹĒ £»
£Ø4£©±Č½ĻµŚ¢ņ½×¶Ī·“Ó¦ĪĀ¶Č£ØT2£©ŗĶµŚ¢ó½×¶Ī·“Ó¦ĪĀ¶Č£ØT3£©µÄøßµĶ£ŗT2 T3 £ØĢī”°<”±”¢”°>»ņ”°=”±£©£¬ÅŠ¶ĻµÄĄķÓÉŹĒ £»
£Ø5£©“ļµ½µŚČż“ĪĘ½ŗāŗ󣬽«ČŻĘ÷µÄĢå»żĄ©“óŅ»±¶£¬¼Ł¶Ø10minŗó“ļµ½ŠĀµÄĘ½ŗā£¬ĒėŌŚĻĀĶ¼ÖŠÓĆĒśĻß±ķŹ¾µŚIV½×¶ĪĢåĻµÖŠBĪļÖŹµÄÅضČĖꏱ¼ä±ä»ÆµÄĒ÷ŹĘ£Ø×¢£ŗÖ»Šė»³öBµÄÅضČĖꏱ¼ä±ä»ÆĒśĻߣ©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
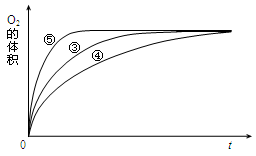
³£ĪĀĻĀ°“ÕÕČēĻĀ·½°øĶź³ÉŹµŃ锣
| ŹµŃ鱹ŗÅ | ·“Ó¦Īļ | “߻ƼĮ |
| ¢Ł | 10mL2% H2O2ČÜŅŗ | ĪŽ |
| ¢Ś | 10mL5% H2O2ČÜŅŗ | ĪŽ |
| ¢Ū | 10mL5% H2O2ČÜŅŗ | 1mL0.1mol”¤L£1FeCl3ČÜŅŗ |
| ¢Ü | 10mL5% H2O2ČÜŅŗ£«ÉŁĮæHClČÜŅŗ | 1mL0.1mol”¤L£1FeCl3ČÜŅŗ |
| ¢Ż | 10mL5% H2O2ČÜŅŗ£«ÉŁĮæNaOHČÜŅŗ | 1mL0.1mol”¤L£1FeCl3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
£Ø1£©25 ”ꏱ£¬ŗĻ³É°±·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗN2£Øg£©+3H2£Øg£© 2NH3£Øg£© ”÷H=£92.4 kJ/mol
2NH3£Øg£© ”÷H=£92.4 kJ/mol
¢ŁŌŚøĆĪĀ¶ČŹ±£¬Č”l mol N2ŗĶ3 mol H2·ÅŌŚĆܱÕČŻĘ÷ÖŠ£¬ŌŚ“߻ƼĮ“ęŌŚĻĀ½ųŠŠ·“Ó¦£¬²āµĆ·“Ó¦·Å³öµÄČČĮæ×ÜŹĒ_______92.4 kJ”£(Ģī”°Š”ÓŚ”±£¬ ”°“óÓŚ”± »ņ”°µČÓŚ”±)
¢ŚŅ»¶ØĢõ¼žĻĀ£¬ÉĻŹöæÉÄę·“Ó¦ŌŚĢå»ż¹Ģ¶ØµÄĆܱÕČŻĘ÷ÖŠ½ųŠŠ£¬ĻĀĮŠŠšŹöÄÜĖµĆ÷·“Ó¦ŅŃ“ļµ½Ę½ŗāµÄŹĒ_______________”£
| A£®NH3Éś³ÉµÄĖŁĀŹÓėNH3·Ö½āµÄĖŁĀŹĻąµČ |
B£®»ģŗĻĘųĢåµÄ·“Ó¦ĖŁĀŹ vÕż£ØNH3£©=vÄę£ØH2£© vÕż£ØNH3£©=vÄę£ØH2£© |
| C£®ČŻĘ÷ÄŚµÄĆÜ¶Č²»ŌŁ±ä»Æ |
| D£®µ„Ī»Ź±¼äÄŚĻūŗÄa mol N2£¬Ķ¬Ź±Éś³É2a mol NH3 |
 Öµ½«_____(Ģī”°Ōö“ó”±£¬ ”°¼õŠ””± »ņ”°²»±ä”±)”£
Öµ½«_____(Ģī”°Ōö“ó”±£¬ ”°¼õŠ””± »ņ”°²»±ä”±)”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ŅŌ»ĘĢśæó(Ö÷ŅŖ³É·ÖŹĒFeS2)ĪŖŌĮĻÉś²śĮņĖįµÄ¹¤ŅÕĮ÷³ĢĶ¼ČēĻĀ£ŗ
(1)Čō“ÓĻĀĮŠĖÄøö³ĒŹŠÖŠŃ”ŌńŅ»“¦ŠĀ½ØŅ»×łĮņĖį³§£¬ÄćČĻĪŖ³§Ö·ŅĖŃ”ŌŚ______µÄ½¼Ēų(Ģī±źŗÅ£©
A.ÓŠ·įø»»ĘĢśæó׏Ō“µÄ³ĒŹŠ B.·ē¹āŠćĄöµÄĀĆÓĪ³ĒŹŠ
C.ĻūŗÄĮņĖįÉõ¶ąµÄ¹¤Ņµ³ĒŹŠ D.ČĖæŚ³ķĆܵÄĪĻƔ¢ÉĢŅµÖŠŠÄ³ĒŹŠ
(2)·ŠĢŚĀÆÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____£¬½Ó“„ŹŅÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ_____”£
(3) ŌŚĮņĖį¹¤ŅµÖĘ·ØÖŠ£¬ĻĀĮŠÉś²ś²Ł×÷ÓėĖµĆ÷Éś²ś²Ł×÷µÄÖ÷ŅŖŌŅņ¶žÕ߶¼ÕżČ·µÄŹĒ_____”£
A. ĮņĢśæóČ¼ÉÕĒ°ŅŖ·ŪĖ飬ŅņĪŖ“óæéµÄ»ĘĢśæó²»ÄÜŌŚæÕĘųÖŠ·“Ó¦
B. “Ó·ŠĢŚĀƳöĄ“µÄĘųĢåŅŖ¾»»Æ£¬ŅņĪŖĀÆĘųÖŠµÄSO2»įÓėŌÓÖŹ·“Ó¦
C. SO2Ńõ»Æ³ÉSO3ŅŖÓĆ“ß»Æ¼Į£¬ÕāŃłæÉĢįøßSO2µÄ×Ŗ»ÆĀŹ
D. SO3ÓĆ98. 3%µÄÅØĮņĖįĄ“ĪüŹÕ£¬ÄæµÄŹĒĪŖĮĖ·ĄÖ¹ŠĪ³ÉĖįĪķ£¬ŅŌĢįó{SO3ĪüŹÕŠ§ĀŹ
(4) ĻĀ±ķŹĒŃ¹Ēæ¶ŌSO2Ę½ŗā×Ŗ»ÆĀŹµÄÓ°Ļģ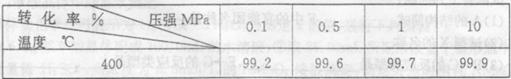
¶ŌÓŚSO2×Ŗ»ÆSO3µÄ·“Ó¦,Ōö“óŃ¹ĒææÉŹ¹×Ŗ»ÆĀŹ______________£¬µ«ŌŚŹµ¼Ź¹¤ŅµÉś²śÖŠ³£²ÉÓĆ³£Ń¹Ģõ¼ž£¬ĄķÓÉŹĒ________________________________”£
(5)ij¹¤³§ÓĆ500tŗ¬ĮņĮæĪŖ48%µÄ»ĘĢśæóÖʱøĮņĖį£¬ČōŌŚ·ŠĢŚĀÆÖŠÓŠ2%µÄFeS2ĖšŹ§,ŌŚ½Ó“„ŹŅÖŠSO3µÄ²śĀŹĪŖ96%,ŌņæɵƵ½98%µÄÅØĮņĖįµÄÖŹĮæŹĒ_____t”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
(14·Ö)¹¤ŅµÖĘĻõĖįµÄÖ÷ŅŖ·“Ó¦ŹĒ4NH3(g)+5O2(g)  4NO(g)+6H2O(g)¦¤H=-akJ/mol(a©0)
4NO(g)+6H2O(g)¦¤H=-akJ/mol(a©0)
(1)Čē¹ū½«4molNH3ŗĶ5molO2·ÅČėČŻĘ÷ÖŠ£¬“ļµ½Ę½ŗāŹ±£¬·Å³öČČĮæ0.8akJ£¬Ōņ·“Ó¦Ź±×ŖŅʵĵē×ÓŹżĪŖ
mol
(2)ČōĘäĖūĢõ¼ž²»±ä£¬ĻĀĮŠ¹ŲĻµĶ¼ÖŠ“ķĪóµÄŹĒ £ØŃ”ĢīŠņŗÅ£©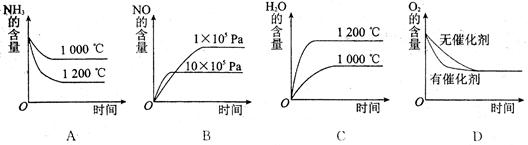
(3)t”ꏱ£¬ŌŚČŻ»ż¹Ģ¶ØµÄĆܱÕČŻĘ÷ÖŠ·¢ÉśÉĻŹö·“Ó¦£¬ČŻĘ÷ÄŚø÷ĪļÖŹµÄÅضČČēĻĀ±ķ
| ÅضČ(mol/L) Ź±¼ä(min) | c(NH3) | c(O2) | c(NO) | c(H2O) |
| Ęš Ź¼ | 4.0 | 5.5 | 0 | 0 |
| µŚ2min | 3.2 | x | 0.8 | 1.2 |
| µŚ4min | 2.0 | 3.0 | 2.0 | 3.0 |
| µŚ6min | 2.0 | 3.0 | 2.0 | 3.0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
1200”ꏱæÉÓĆ·“Ó¦ 2BBr3(g)+ 3H2(g) 2B(s) + 6HBr(g) Ą“ÖĘČ”¾§ĢåÅš”£Ķź³ÉĻĀĮŠĢīæÕ£ŗ
2B(s) + 6HBr(g) Ą“ÖĘČ”¾§ĢåÅš”£Ķź³ÉĻĀĮŠĢīæÕ£ŗ
£Ø1£©ĻĀĮŠĖµ·ØÄÜĖµĆ÷øĆ·“Ó¦“ļµ½Ę½ŗāµÄŹĒ______£ØŃ”ĢīŠņŗÅ£¬ĻĀĶ¬£©”£
a. vÕż(BBr3)= 3vÄę(HBr) b. 2c(H2) = c(HBr)
c.ĆܱÕČŻĘ÷ÄŚŃ¹Ēæ²»ŌŁ±ä»Æ d. ČŻĘ÷ÄŚĘųĢåĘ½¾łÄ¦¶ūÖŹĮæ²»ŌŁ±ä»Æ
£Ø2£©ČōĆܱÕČŻĘ÷Ģå»ż²»±ä£¬ÉżøßĪĀ¶Č£¬¾§ĢåÅšµÄÖŹĮæŌö¼Ó£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ_________”£
a. ŌŚĘ½ŗāŅĘ¶ÆŹ±Õż·“Ó¦ĖŁĀŹĻČŌö“óŗó¼õŠ”
b. ŌŚĘ½ŗāŅĘ¶ÆŹ±Äę·“Ó¦ĖŁĀŹŹ¼ÖÕŌö“ó
c. Õż·“Ó¦ĪŖ·ÅČČ·“Ó¦
d. “ļµ½ŠĀĘ½ŗāŗó·“Ó¦Īļ²»ŌŁ×Ŗ»ÆĪŖÉś³ÉĪļ
£Ø3£©ČōÉĻŹö·“Ó¦ŌŚ10LµÄĆܱÕČŻĘ÷ÄŚ·“Ó¦£¬5minŗó£¬ĘųĢå×ÜÖŹĮæ¼õÉŁ1.1 g£¬ŌņøĆŹ±¼ä¶ĪÄŚĒāĘųµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ__________________”£
£Ø4£©ĶłČŻĘ÷ÖŠ³äČė0.2 mol BBr3ŗĶŅ»¶ØĮæH2£¬³ä·Ö·“Ó¦“ļµ½Ę½ŗāŗ󣬻ģŗĻĘųĢåÖŠHBr°Ł·Öŗ¬ĮæÓėĘšŹ¼ĶØČėH2µÄĪļÖŹµÄĮæÓŠČēĶ¼¹ŲĻµ”£ŌŚa”¢b”¢cČżµćÖŠ£¬H2 µÄ×Ŗ»ÆĀŹ×īøߵďĒ______£ØŃ”Ģī×ÖÄø£©”£bµć“ļµ½Ę½ŗāŗó£¬ŌŁ³äČėH2Ź¹Ę½ŗāµ½“ļcµć£¬“Ė¹ż³ĢÖŠĘ½ŗāŅĘ¶ÆµÄ·½ĻņĪŖ__________£ØĢī”°ÕżĻņ”±”¢”°ÄęĻņ”±»ņ”°²»ŅĘ¶Æ”±£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ŌŚĻĀĮŠŹĀŹµÖŠ£¬Ź²Ć“ŅņĖŲÓ°ĻģĮĖ»Æѧ·“Ó¦µÄĖŁĀŹ£æ
£Ø1£©ČŪ»ÆµÄKClO3·Å³öĘųÅŻŗÜĀż£¬ČöČėÉŁĮæMnO2ŗÜæģ²śÉśĘųĢ唣 ”£
£Ø2£©Ķ¬ÅØ¶Č”¢Ķ¬Ģå»żµÄŃĪĖįÖŠ·ÅČėĶ¬Ńł“󊔵ĊæĮ£ŗĶĆ¾Ģõ£¬²śÉśĘųĢåÓŠæģÓŠĀż”£ ”£
£Ø3£©Ķ¬Ńł“óŠ”µÄŹÆ»ŅŹÆ·Ö±šŌŚ0.1mol”¤L-1µÄŃĪĖįŗĶ1mol”¤L-1µÄŃĪĖįÖŠ£¬·“Ó¦ĖŁĀŹ²»Ķ¬”£ ”£
£Ø4£©¹¤ŅµÉĻ³£½«¹ĢĢåČ¼ĮĻ·ŪĖé½ųŠŠČ¼ÉÕ”£ ”£
£Ø5£©ĻÄĢģµÄŹ³Ę·Ņ×Ć¹±ä£¬¶¬Ģģ¾Ķ²»Ņ×·¢ÉśøĆĻÖĻó”£ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĪŹ“šĢā
£Ø14·Ö£©¹¤ŅµÉĻŅ»°ćŌŚŗćČŻĆܱÕČŻĘ÷ÖŠæÉŅŌ²ÉÓĆĻĀĮŠ·“Ó¦ŗĻ³É¼×“¼£ŗCO(g)+2H2(g) CH3OH(g)
CH3OH(g)
£Ø1£©ÅŠ¶Ļ·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄŅĄ¾ŻŹĒ£ØĢī×ÖÄøŠņŗÅ£©__________
| A£®Éś³ÉCH3OHµÄĖŁĀŹÓėĻūŗÄCOµÄĖŁĀŹĻąµČ | B£®»ģŗĻĘųĢåµÄĆÜ¶Č²»±ä |
| C£®»ģŗĻĘųĢåµÄĻą¶ŌĘ½¾ł·Ö×ÓÖŹĮæ²»±ä | D£®CH3OH”¢CO”¢H2µÄÅØ¶Č¶¼²»ŌŁ·¢Éś±ä»Æ |
| ĪĀ¶Č | 250”ę | 300”ę | 350”ę |
| K | 2.041 | 0.270 | 0.012 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com