
已知H2A是一种无机二元酸,请回答以下问题:
(1) 若H2A为二元弱酸,在水溶液中的电离方程式为 ▲ ;
(2) 若NaHA溶液显碱性,则H2A是 ▲ (填“强酸”、“弱酸”或“无法确定”),原因是 ▲ 。
(3) 若NaHA溶液显酸性,在25℃下,若向0.1 mol·L-1的NaHA溶液中逐滴滴加0.1 mol·L-1 KOH溶液至溶液呈中性。此时该混合溶液中下列关系中,一定正确的是 ▲ ;
a.c(H+)·c(OH-)=1×10-14 b.c(Na+)+c(K+)=0.1 mol·L-1
c.c(Na+)>c(K+) d.c(Na+)=c(HA-)+c(A2-)
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
甘草甜素在治疗丙肝、艾滋病、非典等疾病方面有一定疗效。甘草甜素在一定条件下可转化为甘草次酸。下列有关说法正确的是

A.甘草甜素转化为甘草次酸属于酯的水解
B.在Ni催化作用下,1mol 甘草次酸最多能与2molH2发生加成反应
C.甘草甜素中含有羧基、羰基、碳碳双键、酚羟基等官能团
D.甘草甜素、甘草次酸均可与Na2CO3、溴水等无机试剂发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
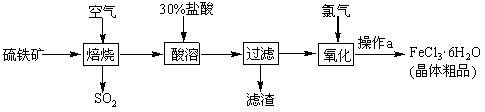
回答下列问题:
(1)煅烧时粉碎硫铁矿的目的是 ,该反应的化学方程式为 。
(2)酸溶及后续过程中均需保持盐酸过量,其目的是 。
(3)操作a为 、过滤、洗涤、干燥,获得FeCl3·6 H2O。
(4)焙烧产生的二氧化硫可以用来生产硫酸,其中利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表:
| 压强/KPa 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% |
| 500 | 93.5% | 96.9% | 97.8% | 99.3% |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |
①根据表中的数据判断该反应的正向属于 (填“放热”或“吸热”)反应,理由是 。
②在400~500℃时,SO2的催化氧化采用常压而不是高压,主要原因是
;
(5)计算每生产1万吨98%硫酸所需要含80% FeS2的 吨(假设反应过程中硫的利用率为90%,结果保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是
A.蛋白质和淀粉都属于天然有机高分子化合物,且淀粉是热值最高的营养物质
B.油脂在氢氧化钠溶液中的水解反应又称为皂化反应
C.加热、加入甲醛或硫酸铜溶液均能使蛋白质变性
D.可以采用多次盐析或渗析的方法来分离、提纯蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
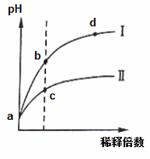
某温度下,pH相同的盐酸和氯化铵溶液分别稀释,pH随溶液
体积变化的曲线如下图所示。据图判断下列叙述中,正确的是
A.Ⅰ为氯化铵稀释时pH值变化曲线,Ⅱ为盐酸稀释时pH值变化曲线
B.b点溶液中水的电离程度比d点溶液中水的电离程度大,但两点的KW相同
C.a点时,等体积的两溶液分别与NaOH反应,消耗的NaOH量相同
D.c点溶液的导电能力一定比b点溶液导电能力强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列试剂的保存方法不正确的是
A.NaOH溶液保存在配有玻璃塞的细口瓶中
B.金属钠通常密封保存在煤油中
C.氯水通常保存在棕色细口瓶并置于阴凉处
D.在盛液溴的试剂瓶中加水,形成“水封”,以减少溴挥发
查看答案和解析>>
科目:高中化学 来源: 题型:
用98%的浓硫酸(密度1.84g · mL-1)配制100mL 1mol·L-1的稀硫酸。现给出下列配制
中可能用到的仪器:①100 mL量筒 ②10 mL量筒 ③50 mL烧杯 ④托盘天平
⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻璃棒。按使用仪器的先后顺序作出的下列排列中正
确的是
A.④③⑥⑦⑤⑥ B.②⑥③⑦⑤⑥
C.①③⑤⑦⑤⑥ D.②③⑥⑦⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列各变化中,E为无色无味的液体(常温下),F为淡黄色粉末,G为常见的无色气体(反应条件均已省略)。回答下列问题:
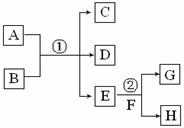 ⑴ 写出反应②的化学反应方程式 ,
⑴ 写出反应②的化学反应方程式 ,
在该反应中,每生成2.24LG(标准状况),该反应转移
电子的物质的量是 。
⑵若反应①在溶液中进行,A、C、D均含氯元素,且A中氯元素的化合价介于C和D之间。则反应①的化学方程式是 。
⑶若反应①在溶液中进行,A是一种强碱,B是一种酸式盐,D是一种无色的气体,且B
遇盐酸产生无色无味的气体。在加热条件下,当A过量时,反应①的离子方程式
是 。
⑷若反应①在溶液中进行,A是一种强酸,B是一种含两种金属元素的盐,当A过量时,C及D均易溶于水。则A过量时反应①的离子反应方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
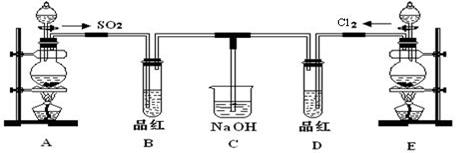
(1)实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后, 漏斗中液体未流下,你认为原因可能是:____________________
(2)实验室用装置E制备Cl2,其反应的化学化学方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。若有6 mol的HCl参加反应,则转移的电子的物质的量为______ mol;被氧化的HCl为 mol。
MnCl2+Cl2↑+2H2O。若有6 mol的HCl参加反应,则转移的电子的物质的量为______ mol;被氧化的HCl为 mol。
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:B:_________________________,D:________________________。
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为 B:_________________________,D:________________________。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示) __________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com