
如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2mol A和1mol B,乙中充入2mol C和1mol He,此时K停在0处。在一定条件下发生可逆反应:2A(g)+B(g) 2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法错误的是
2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法错误的是

A.达到平衡时,甲容器中C的物质的量大于乙容器中C的物质的量
B.根据隔板K滑动与否可判断左右两边的反应是否达到平衡
C.达到平衡后,隔板K最终停留在左侧刻度0~1之间
D.若平衡时K停留在左侧1处,则活塞仍停留在右侧6刻度的右侧
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源:2016-2017学年辽宁省大连市高二上9月月考化学试卷(解析版) 题型:选择题
已知反应A2(g)+2B2(g) 2AB2(g)的△H<0,下列说法正确的是
2AB2(g)的△H<0,下列说法正确的是
A.升高温度,正向反应速率增加,逆向反应速率减小
B.压缩容器体积平衡向正反应方向移动,达到新的平衡后c(A2)变小
C.平衡后加入A2 ,达到新的平衡A2 和B2的转化率均增大
D.达到平衡后,降低温度或增大压强都有利于该反应平衡正向移动
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上学期9月调研化学试卷(解析版) 题型:选择题
某兴趣小组设计如下微型实验装置。实验时,先断开K2,闭合K1,两极均有气泡产生;一 段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是 ( )
段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是 ( )
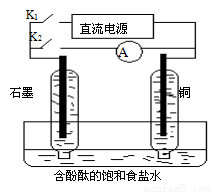
A.断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl- Cl2↑+H2↑
Cl2↑+H2↑
B.断开K2,闭合K1时,石墨电极附近溶液变红
C.断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e—=2Cl—
D.断开K1,闭合K2时,石墨电极作正极
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上学期9月调研化学试卷(解析版) 题型:选择题
在一定温度下 ,向a L密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g)
,向a L密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g) 3Z(g)。此反应达到平衡的标志是( )
3Z(g)。此反应达到平衡的标志是( )
A.容器内压强不随时间变化
B.容器内各物质的浓度不随时间变化
C.容器内X、Y、Z的浓度之比为l∶2∶3
D.单位时间消耗0.1 mol X同时生成0.3 mol Z
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期初考试化学卷(解析版) 题型:填空题
甲醇(CH3OH)是一种重要的化工原料,广泛应用于化工生产,也可以直接用做燃料。
已知:CH3OH(1)+ O2(g) =CO(g) + 2H2O(g) ;△Ha = -443.64 kJ·mol-1
2CO (g) + O2(g) = 2CO2(g) ;△Hb =-566.0 kJ·mol-1
(1)试写出CH3OH(1)在氧气中完全燃烧生成CO2和H2O(g)的热化学方程式: 。
(2) CH3OH和H2的燃烧热分别为△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2和H2为原料合成CH3OH的热化学方程式____________________。
(3)科研人员新近开发出一种由甲醇和氧气以强碱做电解质溶液的新型手机电池,可使手机连续使用一个月才充一次电,据此回答下列问题: 甲醇在 极反应;电极反应式为 。
(4)利用电池可实现电能向化学能转化。某同学设计了一种电解法制取Fe(OH)2的实验装置(如下图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是 (填序号)

A.电源中的a一定为正极,b一定为负极 B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极 D.阴极发生的反应是:2H+ + 2e-→H2↑
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期初考试化学卷(解析版) 题型:选择题
某有机物X的结构简式如图所示,则下列有关说法中正确的是( )
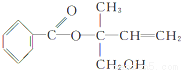
A.X的分子式为C12H16O3
B.X在一定条件下能发生加成、加聚、取代、消去等反应
C.在Ni作催化剂的条件下,1mol X最多只能与1mol H2加成
D.可用酸性高锰酸钾溶液区分苯和X
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期初考试化学卷(解析版) 题型:选择题
下列事实中不能用勒夏特列原理来解释的是( )
A.新制的氯水在光照条件下颜色变浅
B.饱和NaCl溶液中通入HCl气体有晶体析出
C.500℃左右比室温更有利于合成氨反应
D.实验室常用排饱和食盐水的方法收集氯气
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高二上开学测化学卷(解析版) 题型:选择题
t℃时,某一气态平衡体系中含有X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为: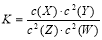 ,有关该平衡体系的说法正确的是( )
,有关该平衡体系的说法正确的是( )
A.升高温度,平衡常数K一定增大
B.升高温度,若混合气体的平均相对分子质量变小,则正反应是放热反应
C.增大压强,W(g)质量分数增加
D.增大X(g)浓度,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上入学考试化学试卷(解析版) 题型:选择题
H2S废气资源化利用途径之一是回收能量并得到单质硫。反应为:2H2S(g) + O2(g) = S2(s) + 2H2O(l) △H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法正确的是

A.电极a为电池的正极
B.电极b上发生的电极反应为:O2+2H2O+4e-===4OH-
C.电路中每通过4mol电子,电池内部释放632kJ热能
D.每17gH2S参与反应,有1mol H+ 经质子膜进入正极区
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com