
密闭容器中进行的可逆反应:aA(g)+bB(g)cC(g)在不同温度(T1和T2)及压强(p1和p2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是 ( )。

A.T1<T2,p1<p2,a+b>c,正反应为吸热反应
B.T1>T2,p1<p2,a+b<c,正反应为吸热反应
C.T1<T2,p1>p2,a+b<c,正反应为吸热反应
D.T1>T2,p1>p2,a+b>c,正反应为放热反应
解析 当图像中有三个变量时,先确定一个量不变,再讨论另外两个量的关系,这叫做“定一议二”。解答该题要综合运用“定一议二”和“先拐先平”的原则。由(T1,p1)和(T1,p2)两条曲线可以看出:①温度相同(T1),但压强为p2时达到平衡所需的时间短,即反应速率大,所以p2>p1;②压强较大(即压强为p2)时对应的w(B)较大,说明增大压强平衡逆向移动,则a+b<c。由(T1,p2)和(T2、p2)两条曲线可以看出:①压强相同(p2),但温度为T1时达到平衡所需的时间短,即反应速率大,所以T1>T2;②温度较高(即温度为T1)时对应的w(B)较小,说明升高温度平衡正向移动,故正反应为吸热反应。
答案 B


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
高锰酸钾分别在酸性、中性、碱性条件下发生的反应如下:
MnO +5e-+8H+===Mn2++4H2O
+5e-+8H+===Mn2++4H2O
MnO +3e-+2H2O===MnO2↓+4OH-
+3e-+2H2O===MnO2↓+4OH-
MnO +e-===MnO
+e-===MnO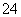 (溶液呈绿色)
(溶液呈绿色)
(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的________影响。
(2)将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为________________________________________________________。
(3)将PbO2投入酸性MnSO4溶液中搅拌,溶液变为紫红色。下列说法正确的是________(填序号)。
a.氧化性:PbO2>KMnO4
b.还原性:PbO2>KMnO4
c.MnSO4溶液可以用盐酸酸化
查看答案和解析>>
科目:高中化学 来源: 题型:
青苹果汁遇碘溶液显蓝色,熟苹果汁能还原银氨溶液,这说明( )
A.青苹果中只含淀粉不含糖类
B.熟苹果中只含糖类不含淀粉
C.苹果转熟时淀粉水解为单糖
D.苹果转熟时单糖聚合成淀粉
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CO(g)+H2O(g)CO2(g)+H2(g) ΔH=-41 kJ
·mol-1。相同温度下,在容积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
| 容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系能量的变化 | |||
| CO | H2O | CO2 | H2 | ||
| ① | 1 | 4 | 0 | 0 | 放出热量:32.8 kJ |
| ② | 0 | 0 | 1 | 4 | 热量变化:Q |
下列说法中,不正确的是 ( )。
A.容器①中反应达到平衡时,CO的转化率为80%
B.容器①中CO的转化率等于容器②中CO2的转化率
C.平衡时,两容器中CO2的浓度相等
D.容器①中CO反应速率等于H2O的反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积不变的密闭容器中进行反应:2SO2(g)+O2(g)2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是 ( )。
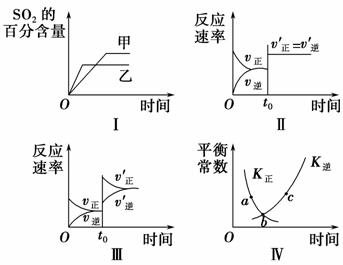
A.图Ⅰ表示温度对化学平衡的影响,且甲的温度较高
B.图Ⅱ表示t0时刻使用催化剂对反应速率的影响
C.图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响
D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A(g)B(g)+C(g)在容积为1.0 L的密闭容器中进行,A的初始浓度为0.050 mol·L-1。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
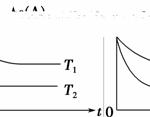
(1)上述反应的温度T1________T2,平衡常数K(T1)________K(T2)。(填“大于”、“小于”或“等于”)
(2)若温度T2时,5 min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为_______________________________________。
②反应的平衡常数K=________________________________________。
③反应在0~5 min区间的平均反应速率v(A)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在1×105Pa、298 K条件下,2 mol H2 燃烧生成水蒸气放出 484 kJ热量,下列热化学方程式正确的是 ( )。
A.H2O(g)===H2 (g) +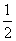 O2(g)
O2(g)
ΔH=+242 kJ·mol-1
B.2H2 (g)+O2 (g) ===2H2O(l)
ΔH=-484 kJ·mol-1
C.H2(g)+1/2O2 (g)===H2O(g)
ΔH=+242 kJ·mol-1
D.2H2(g)+O2 (g) ===2H2O (g)
ΔH=+484 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:常温下,0.01 mol·L-1 MOH溶液的pH为10,MOH(aq)与H2SO4(aq)反应生成1 mol正盐的ΔH=-24.2 kJ·mol-1,强酸与强碱的稀溶液的中和热为ΔH=-57.3 kJ·mol-1。则MOH在水溶液中电离的ΔH为 ( )。
A.-69.4 kJ·mol-1 B.-45.2 kJ·mol-1
C.+69.4 kJ·mol-1 D.+45.2 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
铝是一种重要的金属,在生产、生活中具有许多重要的用途,如下框图是从铝土矿中制备铝的工艺流程: 
已知:①铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;②溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,化学方程式为: 2Na2SiO3+2NaAlO2+4H2O===Na2Al2Si2O8↓+2H2O+4NaOH
回答下列问题:
(1)溶解铝土矿时,发生反应的离子方程式为:____________。
(2)滤渣A的主要成分________;硅铝酸盐沉淀写成氧化物的形式是________。
(3)在工艺流程第三步中,选用二氧化碳作酸化剂而不使用盐酸的原因是_____________
(4)若该工厂用mkg铝土矿共制得nkg Al(假设每步反应进行完全),则铝土矿中Al2O3的质量分数为______。
(5)若将铝溶解,下列试剂中最好选用_______(填编号)。
A.浓硫酸 B. 稀硫酸 C.稀HNO3 D.浓HNO3
(6)电解冶炼铝时用Na3AlF6作助熔剂,Na3AlF6是配合物,其中内界是____,配位数为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com