
配位化合物的数量巨大,组成和结构形形色色,丰富多彩。请指出配合物[Cu(NH3)4](OH)2的中心离子、配体、中心离子的电荷数和配位数 ( )。
A.Cu2+、NH3、+2、4 B.Cu+、NH3、+1、4
C.Cu2+、OH-、+2、2 D.Cu2+、NH3、+2、2
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:
在一定体积的密闭容器中,进行如下化学反应CO2(g)+H2(g)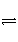
 CO(g)+H2O(g),其
CO(g)+H2O(g),其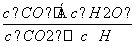 =K,K被称为化学平衡常数,其中K和温度的关系如下表:
=K,K被称为化学平衡常数,其中K和温度的关系如下表:
| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
根据以上信息推断以下说法正确的是( )
A.此反应为放热反应
B.此反应只有达到平衡时,密闭容器中的压强才不会变化
C.此反应达到1 000 ℃时的反应速率比700 ℃时大
D.该反应的化学平衡常数越大,反应物的转化率越低
查看答案和解析>>
科目:高中化学 来源: 题型:
从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平。下列资料表示了三种金属被人类开发利用的大致年限。
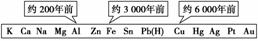
(1)上述资料中的三种常用金属的开发利用之所以有先后,主要取决于________(填选项序号)。
A.金属的导电性强弱
B.金属在地壳中的含量多少
C.金属的化合价高低
D.金属的活动性大小
(2)早在西汉成书的《淮南万毕术》里,就有“曾青得铁则化为铜”的记载。曾青又有空青、白青、石胆、胆矾等名称,其实都是天然的硫酸铜。
①写出“曾青得铁则化为铜”的离子方程式___________________________________________________________________
_________________________________________________________________。
②若根据上述反应设计成原电池,请在方框中画出原电池的装置图,标出正、负极和电解质溶液,并写出电极反应式。

正极反应: ________________________________________________;
负极反应: ______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述中,不正确的是
( )。
A.植物油能使溴的四氯化碳溶液褪色
B.淀粉水解的最终产物是葡萄糖
C.葡萄糖能发生水解反应
D.所有的蛋白质遇浓硝酸均变黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
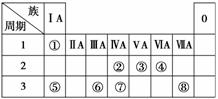
(1)④、⑤、⑥的原子半径由大到小的顺序是__________________________________________________________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
_________________________________________________________________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:___________________________________________________________________
_________________________________________________________________。
(4)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
查看答案和解析>>
科目:高中化学 来源: 题型:
叠氮酸钠(NaN3)是抗甲型H1N1流行感冒药物“达菲”合成过程中的中间活性物质。
(1)NaN3中存在的化学键有________。(答案可能不止一个)
a.离子键
b.极性共价键
c.非极性共价键
(2)3 mol NaN3受撞击会生成4 mol氮气和1 mol离子化合物A,可用于汽车保护气囊。请写出:
①有关反应的化学方程式:___________________________________。
②A的电子式___________________________________________________。
(3)写出与N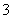 是等电子体的物质的化学式________(两种),等电子体的微粒往往具有相似的结构,试预测N
是等电子体的物质的化学式________(两种),等电子体的微粒往往具有相似的结构,试预测N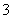 的构型________。
的构型________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
Na2O2(s)+CO2(g)===Na2CO3(s)+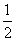 O2(g) ΔH=-226 kJ·mol-1
O2(g) ΔH=-226 kJ·mol-1
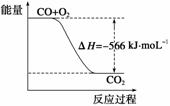
根据以上热化学方程式判断,下列说法正确的是( )
A.CO的燃烧热为283 kJ
B.如图可表示为CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g) ΔH>-452 kJ·mol-1
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
吗丁啉是一种常见的胃药,其有效成分的结构简式如下图所示。
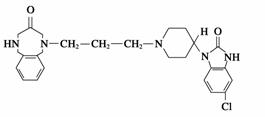
下列关于该物质的说法中正确的是( )
A.该物质属于芳香烃
B.该物质的相对分子质量很大,属于高分子化合物
C.该物质可以发生水解反应和取代反应
D.该物质是一种蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为周期表的一部分,其中的编号代表对应不同的元素。
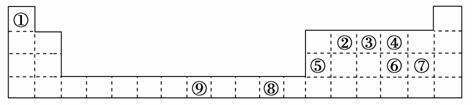
请回答下列问题:
(1)表中属于d区的元素是________(填编号);元素⑧的原子价电子排布式是____________。
(2)③和⑦形成的常见化合物的晶体类型是________;②③④的电负性:________>________>________(用元素符号表示)。判断依据是_________________________________________________________________。
(3)某元素的特征电子排布式(价电子排布式)为nsnnpn+1,该元素为周期表中的________(填编号);该元素与元素①形成的化合物X极易溶于水的原因是__________________________________________________________________
_________________________________________________________________。
(4)②③形成一种超硬、耐磨、耐高温的新型无机非金属材料,则其化学式为________,其熔点比金刚石的________(填“高”或“低”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com