
【题目】短周期的5种主族元素A、B、C、D、E,原子序数依次增大。A、B、C三种元素原子电子层数之和是5;B原子的最外层电子数是其电子层数的2倍;D的一种单质是一种有特殊臭味的淡蓝色气体,可用于杀菌消毒;E与A在同一主族。
请回答下列问题:
(1)A与E可形成化合物甲,甲与水反应可生成H2,写出甲的电子式:__________________。
(2)甲与AlCl3反应得到NaAlH4,甲与NaAlH4都是重要的还原剂,写出NaAlH4与水发生反应的化学方程式:____________________________________。
(3)某同学认为;用惰性气体赶尽反应体系中的空气,将铁和盐酸反应后的气体经浓硫酸干燥,再与E的单质反应,得到固体物质即为纯净的甲;取该固体物质与水反应,若能产生H2;即可证明得到的甲一定是纯净的。判断该同学设想的制备和验纯方法的合理性并说明理由:____________________________________。
(4)C元素的气态氢化物也具有一定的还原性,写出其与CuO反应的化学力程式:____________________________________。
(5)B、D、E组成的一种盐中,B的质量分数为17.91%,其水溶液能使酸性高锰酸钾溶液褪色,写出该盐的化学式:_______________。常温下,该盐的水溶液中离子浓度由大到小的顺序为:____________________________________。
【答案】 ![]() NaAlH4+2H2O==NaAlO2+4H2↑ 制备过程不合理,因为盐酸易挥发,H2中混有HCl,导致产物中有NaCl。验纯的方法不合理,如果有Na残留,Na与水反应也产生H2 2NH3+3CuO
NaAlH4+2H2O==NaAlO2+4H2↑ 制备过程不合理,因为盐酸易挥发,H2中混有HCl,导致产物中有NaCl。验纯的方法不合理,如果有Na残留,Na与水反应也产生H2 2NH3+3CuO![]() 3Cu+N2+3H2O Na2C2O4 c(Na+)>c(C2O42-)>c(OH-)>c(HC2O4-)>c(H+)
3Cu+N2+3H2O Na2C2O4 c(Na+)>c(C2O42-)>c(OH-)>c(HC2O4-)>c(H+)
【解析】本题主要考查元素化合物。根据题意判断A、B、C、D、E分别是氢、碳、氮、氧、钠。
(1)A与E可形成化合物甲,甲与水反应可生成H2,甲的电子式:![]() 。
。
(2)甲与AlCl3反应得到NaAlH4,甲与NaAlH4都是重要的还原剂,NaAlH4与水发生反应的化学方程式:NaAlH4+2H2O==NaAlO2+4H2↑。
(3)判断该同学设想的制备和验纯方法的合理性并说明理由:制备过程不合理,因为盐酸易挥发,H2中混有HCl,导致产物中有NaCl。验纯的方法不合理,如果有Na残留,Na与水反应也产生H2。
(4)C元素的气态氢化物也具有一定的还原性,其与CuO反应的化学力程式:2NH3+3CuO![]() 3Cu+N2+3H2O。
3Cu+N2+3H2O。
(5)B、D、E组成的一种盐中,B的质量分数为17.91%,其水溶液能使酸性高锰酸钾溶液褪色,说明该盐具有还原性,该盐的化学式:Na2C2O4。常温下,该盐的水溶液中![]() 水解,
水解, ![]() +H2O
+H2O![]()
![]() +OH-,溶液中离子浓度由大到小的顺序为:c(Na+)>c(C2O42-)>c(OH-)>c(HC2O4-)>c(H+)。
+OH-,溶液中离子浓度由大到小的顺序为:c(Na+)>c(C2O42-)>c(OH-)>c(HC2O4-)>c(H+)。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A. 分子式为C3H6Cl2的有机物有4种同分异构体(不考虑立体异构)
B. ![]() 和
和![]() 互为同系物
互为同系物
C. 乙炔和溴的四氯化碳溶液反应生成1,2-二溴乙烷
D. 甲苯分子中所有原子都在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1molCu2(OH)2CO3后恰好恢复到电解前的浓度和pH(不考虑CO2的溶解)。则电解过程中共转移电子的物质的量为( )
A.0.4mol
B.0.5mol
C.0.6mol
D.0.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2、CO、CH4、CH3OH等都是重要的能源,也是重要为化工原料。
(1)已知25℃,1.01×105Pa时,8.0g CH4完全燃烧生成二氧化碳气体和液态水放出444.8kJ热量。写出该反应的热化学反应方程式:___________________________________________。
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量及有效地开发利用CO2,工业上可以用CO2来生产燃料甲醇。在体积为2L的密闭容器中,充入lmol CO2和3mol H2,一定条件下发生反应:CO2(g) + 3H2(g) ![]() CH3OH(g) + H2O(g)。经测得CO2和CH3OH(g)的物质的量随时间变化如图所示。
CH3OH(g) + H2O(g)。经测得CO2和CH3OH(g)的物质的量随时间变化如图所示。
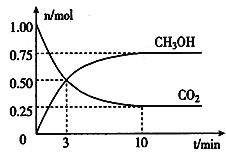
①从反应开始到平衡,CO2的平均反应速率v(CO2)=___________________。
②达到平衡时,H2的转化率为__________。
③该反应的平衡常数K=___________________(表达式)。
④下列措施不能提高反应速率的是__________。
A.升高温度 B.加入催化剂 C.增大压强 D.及时分离出CH3OH
(3)工业上也用CO和H2为原料制备CH3OH,反应方程式为:CO(g) + 2H2(g)![]() CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是______。
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是______。
A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1 mol CO,同时生成1 mol CH3OH
D.CH3OH的质量分数在混合气体中保持不变
E.混合气体的密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.镁条在二氧化碳中不能燃烧B.镁条在氧气或氮气中都能反应
C.镁在空气中燃烧的产物只有氧化镁D.干粉扑灭器可用来扑灭镁燃烧引起的火灾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:N2O4(g)![]() 2NO2(g),将装有N2O4和NO2混合气体的烧瓶浸入热水中,烧瓶内混合气体的颜色逐渐变深。下列结论不能说明该反应已经达到化学平衡状态的是
2NO2(g),将装有N2O4和NO2混合气体的烧瓶浸入热水中,烧瓶内混合气体的颜色逐渐变深。下列结论不能说明该反应已经达到化学平衡状态的是
A. 烧瓶内气体的质量不再变化
B. 烧瓶内气体的颜色不再变化
C. 烧瓶内气体的压强不再变化
D. N2O4的消耗速率与NO2的消耗速率之比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计实验探究H2S的性质,装置如图所示。

下列说法正确的是( )
A. 若F中产生黑色沉淀,则说明H2SO4的酸性比H2S强
B. 若G中产生浅黄色沉淀,则说明H2S的还原性比Fe2+强
C. 若H中溶液变红色,则说明H2S是二元弱酸
D. 若E中FeS换成Na2S,该装置也可达到相同的目的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是( )
A. 丙烯与氯化氢加成的产物有2种 B. 联二苯![]() 的二氯取代物有15种
的二氯取代物有15种
C. 立方烷![]() 的六氯取代物有3种 D. 分子式为CCl2F2的物质只有一种空间结构
的六氯取代物有3种 D. 分子式为CCl2F2的物质只有一种空间结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com