
 常温下用0.100 0mol•L-1的盐酸分别逐滴加入到20.00mL 0.100 0mol•L-1的三种一元碱MOH、XOH、YOH溶液中,溶液的pH随加入盐酸体积的变化如图所示.下列说法正确的是( )
常温下用0.100 0mol•L-1的盐酸分别逐滴加入到20.00mL 0.100 0mol•L-1的三种一元碱MOH、XOH、YOH溶液中,溶液的pH随加入盐酸体积的变化如图所示.下列说法正确的是( )| A. | 分别加入盐酸10 mL时:c(X+)>c(M+)>c(Y+)>c(Cl-) | |
| B. | 分别加入盐酸15 mL时:c(Cl-)>c(X+)>c(MOH)>c(YOH) | |
| C. | 分别加入盐酸至pH=7时:c(X+)=c(M+)=c(Y+) | |
| D. | 将分别加入盐酸20 mL后的三种溶液混合:c(H+)+c(Y+)=c(OH-)+c(X+)+c(MOH) |
分析 常温下用0.100 0mol/L的盐酸分别逐滴加入到20.00mL 0.100 0mol/L的三种一元碱MOH、XOH、YOH溶液中,起始时,三种碱的浓度均为0.1mol/L,根据图象,其中只有XOH的起始pH值为13,则XOH为强碱,MOH和YOH均为弱碱,则XCl为中性,MCl和YCl均会发生水解使溶液呈酸性,根据溶液中的守恒思想,据此分析判断.
解答 解:常温下用0.100 0mol/L的盐酸分别逐滴加入到20.00mL 0.100 0mol/L的三种一元碱MOH、XOH、YOH溶液中,起始时,三种碱的浓度均为0.1mol/L,根据图象,其中只有XOH的起始pH值为13,则XOH为强碱,MOH和YOH均为弱碱,则XCl为中性,MCl和YCl均会发生水解使溶液呈酸性,
A.分别加入盐酸10 mL时,根据图象,三种溶液均为碱性,碱性强弱为XOH-XCl>MOH-MCl>YOH-YCl,表明三种溶液中均是碱电离为主导,使溶液显碱性,碱性越强,电离出的OH-越多,则溶液中离子大小顺序为c(X+)>c(M+)>c(Y+)>c(Cl-),故A正确;
B.分别加入盐酸15 mL时,三种溶液经过反应,起始时均恰好生成c(碱):c(盐)=1:3,考虑到XOH是强碱,则溶液中c(XOH):c(XCl)=1:3,XCl不发生水解,则平衡时c(X+)>c(Cl-),故B错误;
C.分别加入盐酸至pH=7时,溶液中c(H+)=c(OH-),根据电荷守恒,三种溶液中分别存在,c(X+)=c(Cl-),c(Y+)=c(Cl-),c(M+)=c(Cl-),考虑到盐类水解使溶液显碱性,水解程度YCl>MCl,则滴定YOH时消耗的HCl需少一点,XCl不发生水解,三种溶液滴定所需的HCl体积不一样,则不存在关系:c(X+)=c(M+)=c(Y+),正确的关系应为:c(X+)>c(M+)>c(Y+),故C错误;
D.将分别加入盐酸20 mL后的三种溶液混合,恰好起始时为c(XCl)=c(MCl)=c(YCl),根据电荷守恒,c(X+)+c(M+)+c(Y+)+c(H+)=c(Cl-)+c(OH-),根据物料守恒,c(Cl-)=c(X+)+c(M+)+c(MOH)+c(Y+)+c(YOH),c(Y+)+c(YOH)=c(M+)+c(MOH)=c(X+),综合考虑,则有c(H+)+c(Y+)=c(OH-)+c(X+)+c(MOH),故D正确.
故选AD.
点评 本题考查酸碱滴定原理,根据图象判断出XOH是强碱是解题的关键,牢牢把握溶液中的守恒思想,据此分析离子浓度之间的关系,本题需要仔细分析,涉及反应的溶液组分较多,考查综合分析问题的能力,难度不小.


科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、R为原子序数依次增大的六种元素,位于元素周期表的前四周期.B元素原子含有3个能级,且每个能级所含的电子数相同;D的原子核外有8种运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子3d轨道上有4个未成对电子.请回答下列问题:
A、B、C、D、E、R为原子序数依次增大的六种元素,位于元素周期表的前四周期.B元素原子含有3个能级,且每个能级所含的电子数相同;D的原子核外有8种运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子3d轨道上有4个未成对电子.请回答下列问题: ,F基态原子的外围电子排布式3d104s1.
,F基态原子的外围电子排布式3d104s1.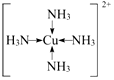 (用元素符号表示).
(用元素符号表示).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 下列有关它的叙述不正确的是( )
下列有关它的叙述不正确的是( )| A. | 能溶于热水 | |
| B. | 在人体内能水解 | |
| C. | 1 mol对乙酰氨基酚与溴水反应时最多消耗Br22mol | |
| D. | 与对硝基乙苯互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 连二次硝酸(H2N2O2)是一种二元酸,常温下,用0.01mol•L-1的NaOH溶液滴定10mL0.01mol•L-1 H2N2O2溶液,溶液pH随加入NaOH溶液体积的变化如图所示,下列有关说法中正确的是( )
连二次硝酸(H2N2O2)是一种二元酸,常温下,用0.01mol•L-1的NaOH溶液滴定10mL0.01mol•L-1 H2N2O2溶液,溶液pH随加入NaOH溶液体积的变化如图所示,下列有关说法中正确的是( )| A. | H2N2O2在水溶液中的电离方程式为H2N2O2═2H++N2O22- | |
| B. | 该滴定过程应该选择甲基橙作为指示剂 | |
| C. | a点的溶液中:c(Na+)+c(H+)═c(OH-)+c(N2O22-)+c(H N2O2-) | |
| D. | b点的溶液中:c(Na+)>c(H N2O2-)>c(OH-)>c(H2N2O2)>c(N2O22-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 25℃时,向盛有50mL pH=3的HA溶液的绝热容器中加入pH=14的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述正确的是( )
25℃时,向盛有50mL pH=3的HA溶液的绝热容器中加入pH=14的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述正确的是( )| A. | HA溶液的物质的量浓度为0.0l mol/L | |
| B. | a→b的过程中,混合溶液不可能存在:c(A-)=c(Na+) | |
| C. | b→c的过程中,温度降低的主要原因是溶液中A-发生了水解反应 | |
| D. | 25℃时,HA的电离平衡常数K约为1.25×10-6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl3溶液中加入KSCN溶液:Fe3++3SCN-═Fe(SCN)3↓ | |
| B. | Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+H2O | |
| C. | 向NaClO溶液中通入少量SO2:2ClO-+SO2+H2O═SO32-+2HClO | |
| D. | 过量的CO2通入水玻璃中:SiO32-+2CO2+2 H2O═H2SiO3↓+2HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com