
| A. | Al2(SO4)3 | B. | SnCl4 | C. | KF | D. | Na2SiO3 |
分析 强酸弱碱盐水解呈酸性,强碱弱酸盐水解呈碱性,配制溶液时,为抑制盐类的水解,往往在溶液中加入适量的酸或碱溶液,以抑制水解,以此解答该题.
解答 解:A.硫酸铝为强酸弱碱盐,铝离子水解生成氢氧化铝,加入硫酸抑制其水解,故A不符合;
B.四氯化锡是强酸弱碱盐,锡离子水解溶液浑浊,加入盐酸抑制其水解,故B不符合;
C.KF为强碱弱酸盐,氟离子水解程度微弱生成氢氧化钾和HF,溶液无变化,不需要加入物质抑制其水解,故C符合;
D.硅酸钠是强碱弱酸盐,水解生成硅酸溶液变浑浊,加入氢氧化钠抑制其水解,故D不符合;
故选C.
点评 本题考查盐类的水解,为高频考点,侧重于学生的分析能力以及基本理论知识的理解与运用的考查,注意把握盐类水解的原理和影响因素,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 可与钠反应 | |
| B. | 可与碳酸钠溶液反应 | |
| C. | 可与溴的四氯化碳溶液发生取代反应 | |
| D. | 可生成高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
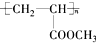
 在铁粉存在下与氯气反应有机产物,只有一种
在铁粉存在下与氯气反应有机产物,只有一种 与足量的NaOH溶液混合,在一定条件下发生反应,消耗NaOH的物质的量为5mol.
与足量的NaOH溶液混合,在一定条件下发生反应,消耗NaOH的物质的量为5mol.| A. | ①③⑤ | B. | ③⑤⑧ | C. | ①④⑧ | D. | ②③⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红色液体 |
| 密度/(g•cm-3) | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
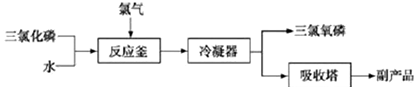


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
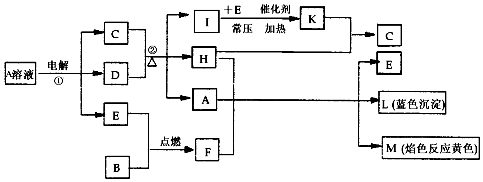
 ,所含化学键为离子键,非极性共价键;
,所含化学键为离子键,非极性共价键;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用石墨电极电解饱和MgCl2溶液:2H2O+2Cl-$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| B. | NH4Al(SO4)2溶液中加入少量的氢氧化钠溶液:Al3++3OH-═Al(OH)3↓ | |
| C. | NaAlO2溶液中通入过量的CO2:Al2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| D. | 用CaSO4治理苏打盐碱地:CaSO4(s)+CO32-(aq)?CaCO3(s)+SO42-(aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇的结构简式为C2H6O | B. | C4H2C18有5种同分异构体 | ||
| C. | 乙酸可以电离,属于离子化合物 | D. | 苯乙烯分子中所有原子可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若两种不同的核素具有相同的中子数,则二者一定不属于同种元素 | |
| B. | 随原子序数的递增,元素原子的核外电子数增多,原子半径逐渐减小 | |
| C. | 在化学反应中,原子首先失去的电子能量最低 | |
| D. | 在元素周期表中,各主族元素的最高化合价与其族序数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com