
常温下,浓度均为0.10mol/L、体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随lg的变化如图所示,下列叙述正确的是
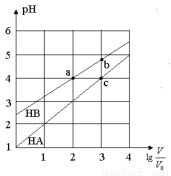
A.相同条件下NaA溶液的pH大于NaB溶液的pH
B.溶液中水的电离程度:a=c>b
C.该温度下HB的电离平衡常数约等于1.11×10-5
D.当lg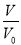 =3时,若两溶液同时升高温度,则
=3时,若两溶液同时升高温度,则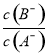 减小
减小
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源:2015-2016学年江苏省高二下第二次月考化学试卷(解析版) 题型:选择题
下列有关氧元素及其化合物表示正确的是( )
A.质子数为8、中子数为10的氧原子:
B.过氧化氢的电子式:
C.氧原子的价电子排布图:
D.次氯酸的结构式:H—Cl—O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁东北育才学校高二下第二段考化学试卷(解析版) 题型:填空题
(1)基态钛原子的价电子排布图为
(2)已知TiCl4在通常情况下是无色液体,熔点为﹣37℃ ,沸点为136℃ ,可知TiCl4为 晶体.
(3)硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示。该阳离子Ti与O的原子数之比为 。
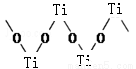
(4)Co的一种氧化物的晶胞如图所示,在该晶体中与一个钴原子等距离且最近的钴原子有 个;筑波材料科学国家实验室一个科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成是 。
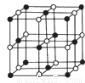

(5)由C、Mg、Ni三种元素组成的一种简单立方结构的化合物具有超导性,其晶胞中C位于体心位置,Mg位于顶角,Ni占据面心位置,该化合物的化学式为 ,晶体中Mg原子周围距离最近的Ni原子有 个,该新型超导材料晶胞参数a=0.38nm,计算该晶体的密度 (g•cm﹣3)(保留三位有效数字)
(6)金属钛晶胞结构如图所示,设钛原子的半径为r,则该晶胞体积的表达式为

查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁东北育才学校高二下第二段考化学试卷(解析版) 题型:选择题
在 分子中,处于同一平面上的碳原子数最多可能有( )
分子中,处于同一平面上的碳原子数最多可能有( )
A.6个 B.8个 C.10个 D.12个
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江哈尔滨六中高三下三模理综化学试卷(解析版) 题型:填空题
[化学—选修3:物质结构与性质]A、B、C、D为原子序数依次增大的四种元素,A2-和B2+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是 (填元素符号),其中C原子的次外层电子排布式为 。
(2)单质A有两种同素异形体,其中沸点高的是 (填分子式),原因是 ;B的氢化物所属的晶体类型是 ,B单质所形成的晶体,一个晶胞平均含有 个原子。
(3)C和D反应可生成组成比为1:5的化合物E,E的分子式为 ,已知该分子的空间构型为三角双锥,则其中两个Cl原子被F原子所替代得到的产物结构有 种。
(4)化合物D2A的立体构型为 ,中心原子的价层电子对数为 ,单质D与Na2SO3溶液反应,其离子方程式为 。
(5)A和B能够形成化合物F,F晶体中的B2+离子的排列方式如图所示,
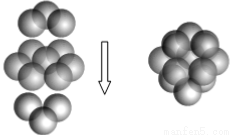
①每个B2+周围最近的等距离的B2+离子有 个。
②已知F的晶胞参数是a0=0.54nm,它的密度为 (只列式不作计算,阿伏加德罗常数为6.02×1023mol-1)。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江哈尔滨六中高三下三模理综化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列有关说法正确的是
A.12g 金刚石中含有的六元碳环数为NA
B.1L1mol/L 的甲醇水溶液中含有氢原子总数为4NA
C.12g 石墨和 C60的混合物中质子总数为6NA
D.反应 KIO3+6HI=KI+3H2O+3I2中,生成1molI2转移电子的总数为2NA
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三考前高考模拟十化学试卷(解析版) 题型:填空题
焦炭与CO、CO2、H2均是重要的化工原料,由CO2制备甲醇过程可能涉及的反应如下:
反应Ⅰ:CO2 (g)+3H2 (g)  CH3OH(g)+H2O(g) △H1 =-49.58kJ·mol -1
CH3OH(g)+H2O(g) △H1 =-49.58kJ·mol -1
反应Ⅱ:CO2 (g)+H2 (g)  CO(g)+H2O(g) △H2 =+41.19kJ·mol -1
CO(g)+H2O(g) △H2 =+41.19kJ·mol -1
反应Ⅲ:CO(g)+2H2(g)  CH3OH(g) △H3
CH3OH(g) △H3
回答下列问题:
(1)反应Ⅲ的△H3 = ,反应Ⅲ自发进行的条件是 (填“较低温”、“较高温”或“任何温度”)。
(2)将焦炭与水蒸气置于容积为2L的密闭容器中发生反应:C(s) +H2O(g)  CO(g)+H2(g),其中H2O、
CO(g)+H2(g),其中H2O、
CO的物质的量随时间的变化曲线如图所示。

①0~1min 内用H2表示该反应的速率为 ,第一个平衡时段的平衡常数是 。
②若反应进行到2min时,改变了温度,使曲线发生如图所示的变化,则温度变化为 (填“升温”或“降温”)。
③反应至5min时,若也只改变了某—个条件,使曲线发生如图所示的变化,该条件可能是下述中的 。
a.加入了C(s) b.加入了水蒸气
c.降低了温度 d.增大了压强
(3)某研究小组将一定量的H2和CO2充入恒容密闭容器中并加入合适的催化剂(发生反应Ⅰ、Ⅱ、Ⅲ),测得了不同温度下体系达到平衡时CO2的转化率(曲线a)及CH3OH 的产率(曲线b),如图所示,请回答问题:
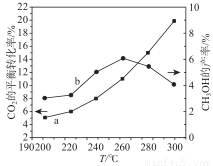
据图可知当温度高于260℃后,CO的浓度随着温度的升高而 (填“增大”、“减小”、“不变”或“无法判断”),其原因是 。
(4)若以CO、O2、K2CO3等构成的熔融盐电池为电源,用惰性电极电解200mL 饱和食盐水,则负极上的电极反应式为 ,当有2.8g燃料被消耗时,电解池中溶液的pH= (常温下,忽略溶液的体积变化,不考虑能量的其他损耗)。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:实验题
现有一份含有FeCl3和FeCl2固体的混合物,为测定FeCl2的含量,进行如下实验:
①称取混合物样品的质量7.06g,将样品溶解
②向溶解后的溶液中,加入足量的双氧水
③再向②所得溶液中加入足量的NaOH溶液,得到红褐色沉淀
④将沉淀过滤、洗涤后,加热灼烧,到质量不再减少,得到固体物质4.00g
根据实验回答下列问题:
(1)样品溶解过程中需加入___________,以防止__________________;
(2)写出溶解后的溶液与双氧水反应的离子方程式____________;
(3)过滤操作中除用漏斗外,还需要的玻璃仪器有____________;
(4)简述检验实验步骤④中沉淀已经洗涤干净的方法____________;
(5)通过实验所得数据,计算固体样品中FeCl2的质量分数:____________;
(6)实验室采用下列装置制取少量无水FeCl3固体。(已知FeCl3固体易潮解,部分夹持仪器已略去。)
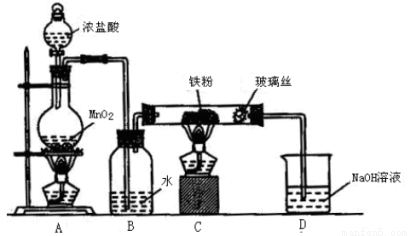
该装置存在明显缺陷,得不到无水FeCl3固体,请你对该装置进行合理的改进:____________。
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三第八次月考理综化学试卷(解析版) 题型:实验题
姜黄素的合成路线如图所示:

已知:①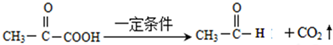
②
请回答下列问题:
(1)D中含有的官能团名称是__________,D→E的反应类型是__________。
(2)姜黄素的结构简式为__________。
(3)反应A→B的化学方程式为__________。
(4)D的催化氧化产物与B可以反应生成一种高分子化合物,其结构简式为__________。
(5)下列有关E的叙述不正确的是__________(填序号).
a.能发生氧化、加成、取代和缩聚反应
b.1molE与浓溴水反应最多消耗3mol的Br2
c.E能与FeCl3溶液发生显色反应
d.1molE最多能与3molNaOH发生反应
(6)G香兰醛(C8H8O3)的同分异构体中,符合下列条件的共有__________种,其中核磁共振氢谱中有4组吸收峰的同分异构体的结构简式为__________
①属于酯类;②能发生银镜反应;③苯环上的一取代物只有2种;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com