
x值 | y=f(x) |
|
|
|
|
|
|
|
|

解析:根据反应物间的定量关系Al3+与OH-的物质的量之比为1∶3时产生Al(OH)3沉淀最多。结合Na2O2与水反应可知此时Al2(SO4)3与Na2O2的物质的量之比为1∶3,生成Al(OH)3沉淀最多,为2 mol;此时Na2O2的物质的量为3 mol。因此0<x≤3阶段,沉淀(y)与Na2O2(x)
符合函数关系式y=2x/3。当Al3+与OH-的物质的量之比为1∶4时恰好沉淀消失,铝元素以![]() 的形式存在,结合Na2O2与水反应可知此时Al2(SO4)3与Na2O2的物质的量之比为1∶4,Na2O2的物质的量为3.2 mol,因此3<x<3.2阶段,沉淀(y)与Na2O2(x)符合函数关系式y=32-10x。
的形式存在,结合Na2O2与水反应可知此时Al2(SO4)3与Na2O2的物质的量之比为1∶4,Na2O2的物质的量为3.2 mol,因此3<x<3.2阶段,沉淀(y)与Na2O2(x)符合函数关系式y=32-10x。
答案:
x值 | y=f(x) |
0<x≤3 | y=2x/3 |
3<x<3.2 | y=32-10x |



 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:高中化学 来源: 题型:阅读理解
| 试验序号 | 实验步骤 | 实验现象 | 结论 |
| ① | 取少量该焰火原料, 加入冷水 |
无明显现象 | 合金中不含Li、Na等活泼金属 合金中不含Li、Na等活泼金属 |
| ② | 取少量该焰火原料, 加入足量稀盐酸 |
完全溶解,有大量气体 产生、溶液呈无色 |
含有能与盐酸反应的较活泼的金属 含有能与盐酸反应的较活泼的金属 |



查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数及物质的量分数。现有下列实验用品:中学化学实验常用仪器、1000 mL烧杯、100 mL量筒、短颈玻璃漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19 g·cm-3)、水。按图示装置进行实验,回答下列问题。(设合金样品完全反应,产生的气体体积不超过100 mL)
(1).补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略):
①将称量后的合金样品用铜网小心包裹好,放在1000 mL烧杯底部,把短颈漏斗倒扣在样品上面。
②_________________________________________________________________________。
③_________________________________________________________________________。
④_________________________________________________________________________。
(2).合金样品用铜网包裹的目的是什么?
________________________________________________________________________。
(3).已知一定质量的铝锌合金的总物质的量为n,实验测得的气体体积为V1mL(已经换算为标准状况)。则铝锌合金中铝的物质的量分数为:_________________。(用含n和V1的式子表示)
(4)本装置也可用于测定金属锌(或其它金属)的相对原子质量,若m g金属锌进行实验,测得的气体体积为V2mL(已经换算为标准状况)。则金属锌的相对原子质量为:_________________。(用含m和V2的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)A、B、D、E 四种短周期元素,其原子序数逐渐增大。A 元素原子的核外电子数、电子层数和最外层电子数均相等,B、D、E 三种元素在周期表中相对位置如图①所示,E 的单质能与水反应生成两种酸。甲、乙、M、W、X、Y、Z 七种物质均由A、B、D 三种元素中的一种或几种组成,其中只有M 分子同时含有三种元素;W 为A、B 两元素组成的18 电子分子,可做火箭燃料;甲、乙为非金属单质;X 分子含有10个电子。它们之间的转化关系如图②。
回答下列问题:
(1)Z的化学式为 。
(2)E 的单质与水反应的离子方程式为 。
(3)W—空气燃料电池是一种碱性燃料电池,电解质溶液是20% ~30%的KOH溶液。W—空气燃料电池放电时,负极反应式为 。
(4)将一定量的A2、B2 的混合气体放入2L密闭容器中,在500°C、2°C×107 Pa下达到平衡。测得平衡气体的总物质的量为0.5mol,其中A2 为0.3mol,B2 为0.1mol。则该条件下A2 的平衡转化率为 ,该温度下反应2BA3(g )3A2(g)+B2(g)的平衡常数为 。
查看答案和解析>>
科目:高中化学 来源:湖南省长郡中学2011届高三分班考试化学试题 题型:填空题
(10分)A、B、D、E 四种短周期元素,其原子序数逐渐增大。A 元素原子的核外电子数、电子层数和最外层电子数均相等,B、D、E 三种元素在周期表中相对位置如图①所示,E 的单质能与水反应生成两种酸。甲、乙、M、W、X、Y、Z 七种物质均由A、B、D 三种元素中的一种或几种组成,其中只有M 分子同时含有三种元素;W 为A、B 两元素组成的18 电子分子,可做火箭燃料;甲、乙为非金属单质;X 分子含有10个电子。它们之间的转化关系如图②。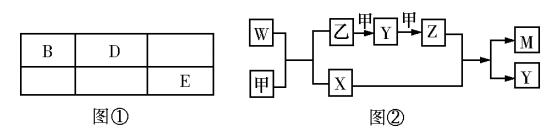
回答下列问题:
(1)Z的化学式为 。
(2)E 的单质与水反应的离子方程式为 。
(3)W—空气燃料电池是一种碱性燃料电池,电解质溶液是20% ~30%的KOH溶液。W—空气燃料电池放电时,负极反应式为 。
(4)将一定量的A2、B2 的混合气体放入2L密闭容器中,在500°C、2°C×107 Pa下达到平衡。测得平衡气体的总物质的量为0.5mol,其中A2 为0.3mol,B2 为0.1mol。则该条件下A2 的平衡转化率为 ,该温度下反应2BA3(g ) 3A2(g)+B2(g)的平衡常数为 。
3A2(g)+B2(g)的平衡常数为 。
查看答案和解析>>
科目:高中化学 来源:2012届四川省成都七中高三下学期二诊模拟理综部分(带解析) 题型:实验题
(14分)测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数及物质的量分数。现有下列实验用品:中学化学实验常用仪器、1000 mL烧杯、100 mL量筒、短颈玻璃漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19 g·cm-3)、水。按图示装置进行实验,回答下列问题。(设合金样品完全反应,产生的气体体积不超过100 mL)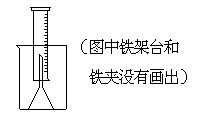
(1).补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略):
①将称量后的合金样品用铜网小心包裹好,放在1000 mL烧杯底部,把短颈漏斗倒扣在样品上面。
②_________________________________________________________________________。
③_________________________________________________________________________。
④_________________________________________________________________________。
(2).合金样品用铜网包裹的目的是什么?
________________________________________________________________________。
(3).已知一定质量的铝锌合金的总物质的量为n,实验测得的气体体积为V1mL(已经换算为标准状况)。则铝锌合金中铝的物质的量分数为:_________________。(用含n和V1的式子表示)
(4)本装置也可用于测定金属锌(或其它金属)的相对原子质量,若m g金属锌进行实验,测得的气体体积为V2mL(已经换算为标准状况)。则金属锌的相对原子质量为:_________________。(用含m和V2的式子表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com