
【题目】在120 ℃时,将a L乙烯、b L乙烷、c L乙炔(b>c)与d L氧气(过量)混合(a+b+c+d=25),点燃使之充分燃烧后,恢复至原来的温度,所得气体的体积可能是
A. 10 L B. 15 L C. 25 L D. 27 L
【答案】D
【解析】
氧气过量时,根据CxHy+(x+y/4)O2![]() xCO2+y/2H2O
xCO2+y/2H2O
将a L乙烯、完全燃烧需要氧气a(x+y/4)=3aL,生成气体的体积为4aL;b L乙烷完全燃烧需要氧气3.5bL生成气体的体积为5bL、c L乙炔完全燃烧需要氧气2.5cL , 生成气体的体积为3cL,剩余氧气为dL-3aL-3.5bL-1.5L, 充分燃烧后,恢复至原来的温度,所得气体的体积是d-3a-3.5b-2.5c+4a +5b +3c=a+d+1.5b+0.5c= a+b+c+d+0.5b-0.5c=25+0.5(b-c)。因为b>c,所以所得气体的体积大于25L。A.10 L不符合题意,不选;B.15 L不符合题意,不选;C.25 L不符合题意,不选; D.27 L符合题意,故D选;答案:D。


科目:高中化学 来源: 题型:
【题目】某小组利用如图所示装置制备少量NCl3。已知:NCl3可由Cl2与NH4Cl溶液在适宜温度下反应生成。常温下,NCl3为黄色油状液体,熔点为-40℃,沸点为71℃;极易爆炸,自然爆炸点为95℃。
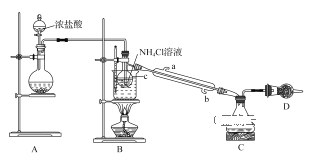
回答下列问题:
(1)装置A中圆底烧瓶内所盛放的固体是___(填化学式)。
(2)装置B中仪器C的名称是___,实验过程中该仪器内发生反应的化学方程式为___。
(3)装置B的烧杯中应控制水浴加热的温度范围为____。
(4)装置D中所盛放的试剂不能为下列选项中的___(填字母)。
a.生石灰 b.NaOH固体 C.碱石灰 d.无水CaCl2
(5)查阅资料可知,电解pH<5的NH4Cl溶液也可制得NCl3,则电解池中产生NCl3的电极为___(填“阴极’’或“阳极’’),该电极的电极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为______,3d能级上的未成对电子数为_______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是________。
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为______,提供孤电子对的成键原子是______。
③氨的沸点_______(填“高于”或“低于”)膦(PH3),原因是_______;氨是______分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______。
(3)铜晶体铜碳原子的堆积方式如图所示。
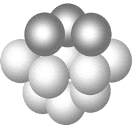
①基态铜在元素周期表中位置__________________。
②每个铜原子周围距离最近的铜原子数目_________。
(4)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如图所示(黑点代表铜原子)。
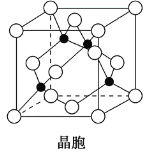
①该晶体的化学式为__________________。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于________(填“离子”或“共价”)化合物。
③已知该晶体的密度为ρ g·cm-3,阿伏加德罗常数为NA,则该晶体中铜原子和M原子之间的最短距离为________pm(只写计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用N2和H2可以实现合成氨气,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产。请回答下列有关问题:
(1)已知N2(g)+O2(g)=2NO(g) ΔH =+180.5kJ·mol-1,N2(g)+3H2(g)![]() 2NH3(g) ΔH =-92.4kJ·mol-1,2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ·mol-1,写出氨气经催化氧化完全生成一氧化氮和水蒸气的热化学方程式为___________。
2NH3(g) ΔH =-92.4kJ·mol-1,2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ·mol-1,写出氨气经催化氧化完全生成一氧化氮和水蒸气的热化学方程式为___________。
(2)在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)![]() 2NH3(g),其化学平衡常数K与温度t的关系如下表:
2NH3(g),其化学平衡常数K与温度t的关系如下表:
t/K | 298 | 398 | 498 | ...... |
K/(mol/L)2 | 4.1×106 | K1 | K2 | ...... |
完成下列问题:
①比较K1、K2的大小:K1______K2(填“>”、“=”或“<”);
②在恒温恒压下判断该反应达到化学平衡状态的依据是______(填序号);
A.2v(H2)(正)=3v(NH3)(逆) B.2v(N2) (正)=v(H2) (逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(3)硝酸工业的尾气NO可用于制备NH4NO3,其工作原理如图。
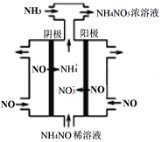
①其阴极的电极反应式为___________。
②常温下,1L pH=6的NH4NO3溶液中c(NH3·H2O)+c(OH-)=________mol·L-1。
(4)工业上生产尿素的化学方程式为:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(l)。在T℃,体积为4L的密闭容器中,通入6mol NH3和3mol CO2,反应达到平衡时,c(NH3)=0.5mol·L-1,c(CO2)=0.25mol·L-1。若此时保持T℃和平衡时容器的压强不变,再向体积可变的容器中充入3mol NH3,则此时反应的v正____ v逆(填“>”“<”或“=”)。再次平衡后,平衡常数为______。
CO(NH2)2(s)+H2O(l)。在T℃,体积为4L的密闭容器中,通入6mol NH3和3mol CO2,反应达到平衡时,c(NH3)=0.5mol·L-1,c(CO2)=0.25mol·L-1。若此时保持T℃和平衡时容器的压强不变,再向体积可变的容器中充入3mol NH3,则此时反应的v正____ v逆(填“>”“<”或“=”)。再次平衡后,平衡常数为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以苯酚为原料的合成路线如下所示,请按要求作答:
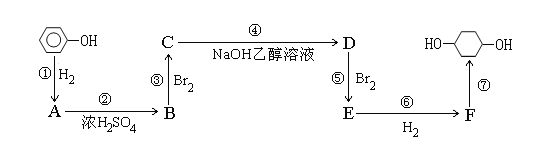
(1)写出A物质的名称:__________;步骤①至⑦中属于加成反应的是__________
(2)写出反应②④的化学反应方程式:
②__________________________________________________________________
④__________________________________________________________________
(3)反应⑤可以制得E,同时得到多种副产物,其中有一种副产物G的结构中只有3种不同的氢原子,副产物G发生图中⑦的反应生成有机物H,写出H结构简式为:__________
(4)1,3-丁二烯是应用广泛的有机化工原料,它还可以用来合成氯丁橡胶。结合以上信息写出以1,3-丁二烯为原料制备氯丁橡胶的单体![]() 的合成路线(必要的无机试剂可任选)。(示例:CH3CH2OH
的合成路线(必要的无机试剂可任选)。(示例:CH3CH2OH ![]() CH2=CH2
CH2=CH2![]() BrCH2CH2Br)___________________________
BrCH2CH2Br)___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W为短周期主族元素,在元素周期表中的相对位置如下图所示,其中Z元素原子之间通常形成Z2分子。下列说法不正确的是( )
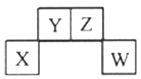
A. X元素的单质既能与强酸反应也能与强碱反应
B. Y元素形成的氢化物在常温下不一定为气体
C. W元素的最高价氧化物对应水化物一定为强酸
D. 由Y、Z、W三种元素形成的二元化合物中只含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
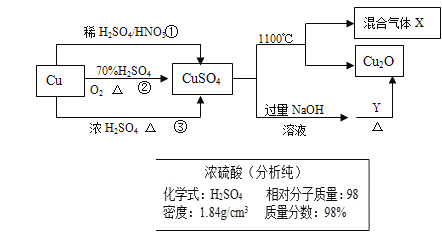
【题目】CuSO4是一种重要化工原料,其制备和有关性质如图所示。
(1)现要用如图所示的浓硫酸来配制步骤①中所需要的1mol/L的稀硫酸480ml,需要用这种浓硫酸的体积为______ml。
(2)配制该稀硫酸所用到的玻璃仪器除玻璃棒、量筒、烧杯外还有_______、__________。
(3)下列操作会使所配溶液浓度偏低的是 _________。
A. 硫酸转移至容量瓶后,没有洗涤烧杯
B. 未冷却至室温就转移至容量瓶
C. 容量瓶中存在少量蒸馏水
D. 定容时俯视刻度 E.量取浓硫酸时量筒内有少量蒸馏水
(4)制取硫酸铜的途径①②③中,途径_________能更好地体现绿色化学的思想。
(5)配制1000ml 0.1mol/L的硫酸铜溶液,需用托盘天平称取________g胆矾。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备下列物质的生产流程合理的是( )
A. 由铝土矿冶炼铝:铝土矿![]() Al2O3
Al2O3![]() AlCl3
AlCl3![]() Al
Al
B. 从海水中提取镁:海水![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
C. 由NaCl制漂白粉:饱和食盐水![]() Cl2
Cl2![]() 漂白粉
漂白粉
D. 由黄铁矿制硫酸:黄铁矿![]() SO2
SO2![]() SO3
SO3![]() H2SO4
H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为CaF2、H3BO3(层状结构,层内的H3BO3分子通过氢键结合)、金属铜三种晶体的结构示意图,请回答下列问题:
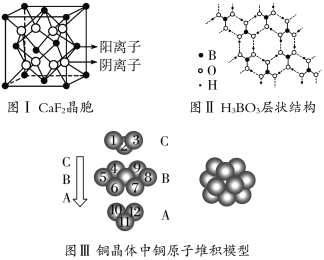
(1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为________,图Ⅲ中未标号的铜原子形成晶体后周围最紧邻的铜原子数为________。
(2)图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是________,H3BO3晶体中B原子个数与极性键个数比为________。
(3)三种晶体中熔点最低的是________,其晶体受热熔化时,克服的微粒之间的相互作用为________________________________________________________________。
(4)结合CaF2晶体的晶胞示意图,已知,两个距离最近的Ca2+核间距离为a×10-8 cm,计算CaF2晶体的密度为________g·cm-3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com