
分析 (1)Ge原子核外电子数为14+18=32,结合能量最低原理书写核外电子排布式;
(2)Sn是金属,形成金属晶体;
(3)①根据价层电子对互斥理论确定其空间构型,非金属元素之间易形成共价键;
(4)二氧化硅是原子晶体,每个硅原子和4个氧原子之间形成4个共价键,每个氧原子和2个硅原子形成2个共价键;
(5)含有空轨道和孤电子对的原子之间易形成配位键;
(6)碳氧键的红外伸缩振动频率与键的强度成正比.
解答 解:(1)Ge原子核外电子数为14+18=32,根据构造原理可知核外电子排布式为1s22s22p63s23p63d104s24p2,
故答案为:1s22s22p63s23p63d104s24p2;
(2)金属元素能形成金属晶体,所以能形成金属晶体的是Sn,
故答案为:Sn;
(3)二氧化碳分子中碳原子价层电子对数是2,且不含孤电子对,所以其空间构型是直线形,碳原子和氧原子之间存在共价键,
故答案为:直线形,共价键;
(4)二氧化硅是原子晶体,每个硅原子和4个氧原子之间形成4个共价键,1molSiO2晶体中的硅氧键数目为4mol,
故答案为:4mol;
(5)Ni原子中含有空轨道、CO中含有孤电子对,所以二者能形成配位键,
故答案为:配位键;
(6)Ni(CO)4中碳氧键的伸缩振动频率为2060cm-1,CO分子中碳氧键的伸缩振动频率为2143cm-1,碳氧键的红外伸缩振动频率与键的强度成正比,则Ni(CO)4中碳氧键的强度与CO分子中碳氧键的强度弱,
故选:B.
点评 本题考查物质结构和性质,涉及核外电子排布、晶体类型与结构、空间构型、化学键、配位键等,比较基础,注意识记中学常见晶体结构.


科目:高中化学 来源:2016-2017学年浙江省高一上第一次质检化学卷(解析版) 题型:选择题
某元素的一种同位素X 的质量数为A,含N个中子,它与1H 原子组成HmX分子,在ag HmX 中所含质子的物质的量是
A. 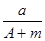 (A-N+m)mol B.
(A-N+m)mol B. 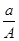 (A-N)mol
(A-N)mol
C. 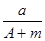 ( A-N)mol D.
( A-N)mol D. 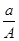 (A-N+m)mol
(A-N+m)mol
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有4种不同的伸展方向 | B. | 有5种不同能量的电子 | ||
| C. | 有5种不同的运动范围 | D. | 有14种不同运动状态的电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10mol 10% | B. | 20mol 20% | C. | 20mol 40% | D. | 30mol 80% |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 增加FeS2的量 | B. | 增大O2的浓度 | C. | 升高温度 | D. | 减小压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
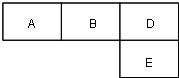 M、A、B、D、N、E五种短周期元素的原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在如图(周期表的一部分)占有相应的位置,它们的原子序数之和为37.
M、A、B、D、N、E五种短周期元素的原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在如图(周期表的一部分)占有相应的位置,它们的原子序数之和为37.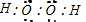 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 加热煮沸的主要目的是除去溶液中溶解的氧气 | |
| B. | 稀释过程中用到的玻璃仪器主要有烧杯、玻璃棒、胶头滴管 | |
| C. | 滴定过程中可用淀粉溶液作指示剂 | |
| D. | 铁矿石中铁的质量分数为70% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com