
| A.向某溶液中加入Na2CO3溶液,若有白色沉淀生成,证明一定含有Ca2+ |
| B.向某固体中加入稀盐酸,产生了无色气体,证明该固体一定含有CO32— |
| C.向某溶液中滴加KSCN溶液,若溶液出现红色则说明原溶液中含Fe3+ |
| D.向某溶液中先加稀硝酸,再加BaC12溶液,生成白色沉淀,证明一定含有SO42— |
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源:不详 题型:单选题
| | 物质 | 杂质 | 试剂 | 主要操作 |
| A | SiO2 | Fe2O3 | 盐酸 | 过滤 |
| B | NaHCO3 | NH4Cl | — | 加热 |
| C | 铁粉 | 铜粉 | 稀硫酸 | 过滤 |
| D | 甲烷 | 乙烯 | 溴水 | 蒸馏 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
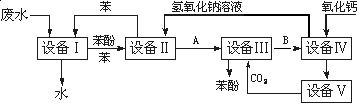
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用结晶法提纯混有少量氯化钾的硝酸钾 |
| B.用KSCN检验溶液中Fe3+的存在 |
| C.用湿润的淀粉碘化钾试纸检验氯气 |
| D.用酒精萃取碘水中的碘 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
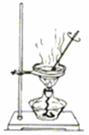 | 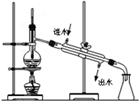 |  | 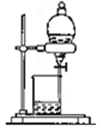 |
| A.从NaCl溶液提取NaCl固体 | B.实验室中制取少量蒸馏水 | C.闻氯气的气味 | D.分离油和水混合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 操作 | 现象 | 结论 |
| A | 向某无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| B | 向某溶液中先滴加KSCN溶液,再滴加少量氯水 | 先无明显现象,后溶液变成血红色 | 原溶液中含有Fe2+和Fe3+ |
| C | 将铜片放入浓硝酸中 | 产生大量红棕色气体,溶液变为蓝绿色 | 浓硝酸有强氧化性和酸性 |
| D | 向Na2SiO3溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2 min后,试管里出现凝胶 | 酸性:硅酸>盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
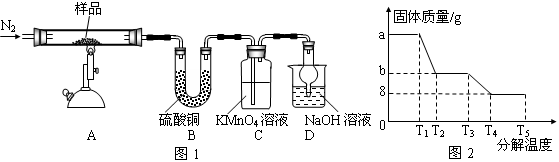
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 湿润的KI淀粉试纸 | 湿润的红色石蕊试纸 |
| A | NO2 | NH3 |
| B | H2S | HCl |
| C | Cl2 | CO2 |
| D | SO2 | NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com